Märkimisväärsed võimalused penitsilliinide täiustamiseks avanesid nende struktuurse aluse - 6-aminopenitsillaanhappe - vabanemisega.
6-aminopenitsillaanhape saadakse bensüülpenitsilliini ensümaatilise lõhustamise (imidaaside) ja keemilise deatsüülimise teel. 6-aminopenitsillaanhappe keemilised modifikatsioonid viidi läbi erinevate radikaalide lisamisega aminorühma. Uuringu eesmärk oli luua teatud omadustega poolsünteetilised penitsilliinid:
a) resistentne mitmete mikroorganismide poolt toodetava penitsillinaasi (β-laktamaasi) toimele;
b) happeresistentsed ravimid, mis on efektiivsed suukaudsel manustamisel;
c) laia toimespektriga penitsilliinid.
Oluline samm oli penitsilliinide suhtes resistentsete penitsilliinide väljatöötamine1. Selle omadusega poolsünteetiliste penitsilliinide hulka kuuluvad oksatsilliini naatriumsool, dikloksatsilliin ja mõned teised. Nende ravimite väärtuse määrab asjaolu, et need on tõhusad bensüülpenitsilliini suhtes resistentsete stafülokokkide tüvede vastu (nende tüvede penitsillinaasi tootmise tõttu).
Oksatsilliini puhul kombineeritakse resistentsus penitsillinaasi suhtes resistentsusega happelises keskkonnas. Antimikroobse toime spektri järgi on see sarnane bensüülpenitsilliiniga. Märkimisväärne osa seondub plasmavalkudega (> 90%). Ravim ei tungi läbi hematoentsefaalbarjääri. See eritub peamiselt neerude kaudu. Manustamissagedus on iga 4-6 tunni järel.
Penitsillinaasi toimele resistentsete ravimite rühma kuulub ka naftsilliin, millel on kõrge antibakteriaalne toime ja mis tungib läbi vere-aju barjääri. See eritub peamiselt sapiga, vähemal määral - neerude kaudu. Manustatakse enteraalselt ja parenteraalselt.
Laia toimespektriga poolsünteetilised penitsilliinid jagunevad järgmistesse rühmadesse:
I. Ravimid, mis ei mõjuta Pseudomonas aeruginosa
Aminopenitsilliinid
Ampitsilliin Amoksitsilliin
II. Pseudomonas aeruginosa vastu aktiivsed ravimid Karboksüpenitsilliinid Karbenitsilliin Tikartsilliin Karfetsilliin Ureidopenitsilliinid Piperatsilliin Aslotsilliin Metsotsilliin
Üks meditsiinipraktikas laialdaselt kasutatavatest aminopenitsilliinidest on ampitsilliin. See mõjutab mitte ainult grampositiivseid, vaid ka gramnegatiivseid mikroorganisme (salmonella, shigella, mõned Proteuse tüved, Escherichia coli, Friedlanderi batsill, gripibatsill). Gram-positiivsete bakterite osas on see aktiivsuselt madalam kui bensüülpenitsilliinil (nagu kõik teised poolsünteetilised penitsilliinid), kuid parem kui oksatsilliini. Penitsillinaasi poolt hävitatud ja seetõttu penitsillinaasi moodustavate stafülokokkide vastu ebaefektiivne. Ampitsilliin on happekindel. Alates seedetrakti imendub mittetäielikult (biosaadavus ~ 40%) ja aeglaselt. See seondub vähesel määral (10-30%) plasmavalkudega. Läbi vere-aju barjääri tungib paremini kui oksatsilliin. Peamiselt eritub neerude kaudu. Ampitsilliini manustatakse 4-8 tunniste intervallidega.Ravim on madala toksilisusega ja patsientidele hästi talutav.
Toodetakse kombineeritud ravimit Ampiox (ampitsilliin oksatsilliiniga).
Amoksitsilliin on aktiivsuselt ja toimespektrilt sarnane ampitsilliiniga, kuid imendub soolestikust täielikumalt. Sisestage see ainult enteraalselt.
Loetletud poolsünteetilisi laia toimespektriga penitsilliinid, mis on aktiivsed Pseudomonas aeruginosa vastu, hävitatakse penitsillinaasiga.
Karbenitsilliin (piopeen) on oma antimikroobse toimespektri poolest sarnane ampitsilliiniga. See erineb sellest selle poolest, et see toimib aktiivselt igat tüüpi proteusidele ja Pseudomonas aeruginosale. (Pseudomonas aeruginosa).
Mao happelises keskkonnas ravim hävib; imendub vähesel määral. Seetõttu manustatakse seda intramuskulaarselt ja intravenoosselt. Umbes 50% valmistoidust
Rata seondub plasmavalkudega. See ei tungi hästi läbi hematoentsefaalbarjääri. See eritub neerude kaudu (sekretsioon ja filtreerimine) ning osaliselt maksa kaudu. Toime kestus on 4-6 tundi.
Loodud uus ravim- karbenitsilliin-indanüülnaatrium, mis on happekindel ja mõeldud enteraalseks manustamiseks (infektsioonide korral kuseteede).
Ravimid karfetsilliin ja tikartsilliin on oma omadustelt sarnased karbenitsilliiniga. Karfetsilliin, erinevalt karbenitsilliinist, on happekindel ja seda manustatakse suu kaudu. Tikartsilliin on mõnevõrra aktiivsem kui karbenitsilliin, eriti selle mõju poolest Pseudomonas aeruginosale.
Ureidopenitsilliinide antibakteriaalne toime on sarnane karboksüpenitsilliinide omaga. Suhtes Klebsiella ureidopenitsilliinid on tõhusamad. Vastavalt toimele Pseudomonas aeruginosale võib ravimid järjestada järgmisesse ritta (kahanevas järjekorras): aslotsilliin = piperatsilliin> metsotsilliin = tikartsilliin> karbenitsilliin.
Oluliseks probleemiks on paljude mikroorganismide resistentsuse ületamine β-laktaamantibiootikumide suhtes, mis on tingitud teatud tüvede võimest toota β-laktamaase. Nende andmete põhjal sünteesiti spetsiifilised β-laktamaasi inhibiitorid (klavulaanhape, sulbaktaam, tasobaktaam), et vältida selle antibiootikumide rühma hävimist. β-laktamaasi inhibiitorid on osa paljudest kombineeritud preparaatidest (β-laktaamantibiootikumid + β-laktamaasi inhibiitorid).
Üks laialdaselt kasutatavaid ravimeid on Augmentin (amoksitsilliin + klavulaanhape). Nagu juba märgitud, on amoksitsilliin laia toimespektriga bakteritsiidne β-laktaamantibiootikum. Klavulaanhape (toodetud Streptomyces clavuligerus) kehtib ka β-laktaami derivaatide kohta. Kuid antibakteriaalne toime väljendub temas väga mitte suur kraadi. Peamine toime on paljude β-laktamaaside konkureeriv pöördumatu pärssimine. Mõne poolt toodetud β-laktamaasidel Enterobakterid, See ei tööta.
Augmentinil on lai antibakteriaalne spekter, sealhulgas β-laktamaasi tootvad grampositiivsed bakterid (stafülokokid ja enamik streptokokke, sealhulgas enterokokid) ja gramnegatiivsed bakterid (N. gonorrhoeae, N. meningitidis, N. influenzae, Gardenella vaginalis, Bordetella pertussis, E. coli, Klebsiella kopsupõletik, Proteus mirabilis, Salmonella). Täheldati kõrget efektiivsust paljude β-laktamaase tootvate anaeroobsete bakterite tüvede vastu.
Ravimit manustatakse tavaliselt enteraalselt 1 kord päevas. Imendub hästi (74-92%). Biosaadavus umbes 70%. Ained ja nende metaboliidid erituvad neerude kaudu.
Kasutatakse infektsioonide korral hingamisteed, kuseteede, kell bakteriaalne kahjustus nahk ja pehmed koed, luud, liigesed, septilistes tingimustes.
Loodud on ka teisi kombineeritud preparaate: unasiin (ampitsilliin + sulbaktaam), amoksiklav (amoksitsilliin + klavulaanhape), tasotsiin (piperatsilliin + tasobaktaam) jne.
Sünteesitud "ebatüüpiline" ravim penitsilliini pevmetsillinaam, mis toimib peamiselt gramnegatiivsetele bakteritele. See on eelravim. Organismis moodustub sellest metsillinaam. Määrake ravim sees, kuid see imendub halvasti.
Poolsünteetilised penitsilliinid oksatsilliin, dikloksatsilliin, naftsilliin on eelistatud ravimid penitsillinaasi tootvate stafülokokkidega nakatumisel, s.o. bensüülpenitsilliini suhtes resistentne. Oksatsilliini manustatakse suu kaudu ja intramuskulaarselt, naftsilliini - suukaudselt, intramuskulaarselt ja intravenoosselt.
Laia toimespektriga ampitsilliin pakub suurimat huvi gramnegatiivsete mikroorganismide või segafloora põhjustatud haiguste ravina. Seda kasutatakse suukaudselt kuseteede, sapiteede, hingamisteede, seedetrakti infektsioonide korral, mädase kirurgilise infektsiooni korral. Ampitsilliini (pentreksiili) naatriumsoola manustatakse intramuskulaarselt ja intravenoosselt. Amoksitsilliinil on sarnased näidustused taotlusele. Sisestage see enteraalselt.
Karbenitsilliin, karfetsilliin, tikartsilliin, aslotsilliin ja teised selle rühma ravimid on eriti näidustatud Pseudomonas aeruginosa, Proteus, Escherichia coli (püelonefriidi, kopsupõletiku, septitseemia, peritoniidi jne) põhjustatud infektsioonide korral.
Esindada lai rühm hallitusseente kolooniate poolt sünteesitud antibiootikumid Penicillium; kuuluvad nn β-laktaamantibiootikumide hulka. Penitsilliinid on esimesed antibiootikumid, mida praktilises meditsiinis kasutatakse. Need on aktiivsed enamiku grampositiivsete ja ka mõnede gramnegatiivsete bakterite (gonokokid, meningokokid ja spiroheedid) vastu.
Päritolu järgi eristatakse looduslikke ja poolsünteetilisi penitsilliine.
Biosünteetilised (looduslikud) penitsilliinid: bensüülpenitsilliini naatriumsool (penitsilliini teva); bensüülpenitsilliini kaaliumisool; bensüülpenitsilliini novokaiini sool (abbotsilliin, biotsilliin, novotsilliin, protsilliin, duratsilliin); bensatiinbensüülpenitsilliin (bitsilliin-1, ekstentsilliin); bensatiinbensüülpenitsilliin + bensüülpenitsilliin novokaiinisool (bitsilliin-5, dissilliin-5); fenoksümetüülpenitsilliin (rõuged). Poolsünteetilised penitsilliini antibiootikumid: amidinopenitsilliinid (amdinotsilliin, pivamdinotsilliin, bakamdinotsilliin, atsidotsilliin); isoksasolpenitsilliinid (oksatsilliin, kloksatsilliin, flukloksatsilliin); aminopenitsilliinid (amoksitsilliin, ampitsilliin); karboksüpenitsilliinid (tikartsilliin, karfetsilliin, karbenitsilliin); ureidopenitsilliinid (metsotsilliin, aslotsilliin, piperatsilliin).
looduslikud penitsilliinid
Looduslikest penitsilliinidest kasutatakse ravimit laialdaselt bensüülpenitsilliin saadud haljashallitusest Penicillium. See ravim on võimeline pärssima streptokokkide, stafülokokkide, gonokokkide, pneumokokkide, kahvatu spiroheedi, gaasigangreeni, teetanuse ja siberi katk. Bensüülpenitsilliini manustatakse eranditult parenteraalselt (peamiselt intramuskulaarselt), kuna ravim hävib mao happelises keskkonnas.
Enamikul looduslikel penitsilliinidel on mitmeid olulisi puudusi. Peamised neist on:
- kitsas spekter antibakteriaalne toime(peamiselt grampositiivsed mikroorganismid);
- vastuvõtu kõrge sagedus lühikese toimeaja tõttu (välja arvatud bitsilliinid);
- ainult parenteraalne manustamine mao happelises keskkonnas hävimise tõttu (välja arvatud fenoksümetüülpetsilliin);
- neid hävitab ensüüm penitsillinaas (β-laktamaas).
Grampositiivsete ja gramnegatiivsete mikroorganismide β-laktamaasi tootmise iseloom on erinev, mis mõjutab nende tundlikkust penitsilliini antibiootikumide suhtes ja viimaste toimespektrit. Seega hakkavad grampositiivsed bakterid β-laktamaasi sekreteerima alles pärast antibiootikumide keskkonda sattumist ning gramnegatiivsete mikroorganismide puhul on tüüpiline ensüümi püsiv süntees, st olenemata ravimi olemasolust keskkonnas. Seetõttu on viimased esialgu valmis antibiootikumiga kohtuma ja selle hävitades näitavad ravimi suhtes resistentsust. Lisaks hõlbustavad gramnegatiivsete bakterite õhem rakusein ja poriinikanalid antibiootikumide tungimist rakku, kus need β-laktamaasid hävitavad. Nende omaduste tõttu on gramnegatiivsed bakterid β-laktaamantibiootikumide suhtes resistentsemad.
Selle mikroobide resistentsuse ületamiseks on penitsilliinid hiljuti kombineeritud β-laktamaasi inhibiitoritega, nagu klavulaanhape, sulbaktaam ja tasobaktaam. Sellise kombinatsiooni näited ravimid on poolsünteetiliste penitsilliinide preparaadid: amoksitsilliin + klavulaanhape (amoksiklav, augmentiin), ampitsilliin + sulbaktaam (unasiin, supatsipiin), piperatsilliin + tasobaktaam (tütotsiin, zosiin). Tänu oma kõrgele antibakteriaalsele toimele on need kombineeritud preparaadid kliinilises praktikas kindlalt juurdunud.
Poolsünteetilised penitsilliini antibiootikumid
Poolsünteetilistel penitsilliinidel on ka mõned puudused, eelkõige:
- Amidinopenitsilliini derivaatidel (amdinotsilliin, pivamdinotsilliin, bakamdinotsilliin, atsidotsilliin) on kitsas toimespekter. Inhibeerivad tõhusalt gramnegatiivseid baktereid (E. coli, Shigella, Salmonella, Klebsiella), kuid ei ole aktiivsed grampositiivsete mikroorganismide vastu.
- Isoksasolpenitsilliini derivaadid - oksatsilliin (prostafliin), kloksatsilliin, flukloksatsilliin - ühendavad suhteliselt kitsa antibakteriaalse toime spektri resistentsusega β-laktamaasi suhtes.
- Aminopenitsilliini derivaadid - amoksitsilliin (flemoxin salutab), ampitsilliin (ampic, ampyrex jne) - on üsna laia toimespektriga, kuid penitsillinaas hävitab need.
- Karboksüpenitsilliini derivaadid – tikartsilliin, karfetsilliin, karbenitsilliin ja ureidopeniailliin metslotsilliin, aslotsilliin (sekuropen), piperatsilliin (pipraks, piperatsiil jt) – on aktiivsed enamiku tuntud bakterite, sealhulgas Pseudomonas aeruginosa vastu, kuid penitsillinaas hävitab need.
Väga populaarne on ravim Ampiox (Xxami), mis on ampitsilliini ja oksatsilliini kombinatsioon. See antibiootikumide kombinatsioon võimaldab teil iga üksiku ravimi eeliste tõttu suurendada toimespektrit.
Penitsilliini antibiootikumide kõrvaltoimed
Penitsilliini antibiootikumid on endiselt peamine ravi ravimite rühm kroonilised haigused hingamiselundid. Neid antibiootikume kasutatakse laialdaselt kuse- ja sapiteede, seedetrakti nakkushaiguste ravis, mädaste kirurgiliste infektsioonide korral jne. Lisaks on penitsilliinid väga tõhusad süüfilise kõikides staadiumides. Penitsilliini antibiootikume iseloomustab madal toksilisus ja lai valik terapeutiline toime.
Peamine kõrvalmõjud penitsilliini antibiootikumid on allergilised reaktsioonid, mille raskusaste võib olla erinev: nahalööbest kuni raskete vormideni, millega kaasneb limaskestade turse, artriit, neerukahjustus jne. Ohtlik ja kiiresti arenev allergiline reaktsioon (20 minuti jooksul pärast penitsilliini süstimist) on anafülaktiline šokk. Õigeaegse puudumisel arstiabi saadaval surma. Ravi seisneb antibiootikumi kaotamises ja glükokortikoidide, antihistamiinikumide ja põletikuvastaste ravimite, kaltsiumkloriidi ja mitmete teiste ravimite kasutuselevõtmises. Kell anafülaktiline šokk koos loetletud vahenditega on näidatud epinefriini kasutamine.
Lisaks allergilistele reaktsioonidele kipuvad penitsilliinid ärritav toime. Suurtes annustes (või otse tserebrospinaalvedelikku süstituna) kasutamisel võivad penitsilliinid põhjustada neurotoksilist toimet. Happekindlate penitsilliinide võtmine võib põhjustada düsbakterioosi. Üldiselt on kõik penitsilliini antibiootikumid suhteliselt hästi talutavad.
Allikad:
1. Farmakoloogia loengud kõrgematele meditsiini- ja farmaatsiaharidus/ V.M. Brjuhanov, Ya.F. Zverev, V.V. Lampatov, A. Yu. Žarikov, O.S. Talalaeva - Barnaul: kirjastus Spektr, 2014.
2. Farmakoloogia koos koostisega / Gaevy M.D., Petrov V.I., Gaevaya L.M., Davydov V.S., - M.: ICC märts, 2007.
Hetkel sees Venemaa Föderatsioon probleem on üsna terav ratsionaalne valik antibakteriaalne ravim erinevate nakkushaiguste korral. Penitsilliinid on endiselt kõige tuntum antibiootikumide rühm.
Praegu eristatakse:
- Biosünteetilised penitsilliinid: bensüülpenitsilliin (naatrium, kaalium, novokaiin, etüleendiamiini soolad); bitsilliinid (1 ja 5); fenoksümetüülpenitsilliin, bensüülpenitsilliin bensatiin.
- Poolsünteetilised penitsilliinid:
- I. Põlvkond:
- penitsillinaasiresistentsed (isoksasolüülpenitsilliinid): metitsilliin, oksatsilliin, dikloksatsilliin, kloksatsilliin, naftsilliin;
- penitsilliiniresistentsed (aminopenitsilliinid): ampitsilliin, amoksitsilliin, bakampitsilliin, penametsilliin;
- kombineeritud: augmentiin (amoksitsilliin + klavulaanhape), sultamitsilliin (ampitsilliin + sulbaktaam).
- II. Põlvkond (karboksüpenitsilliinid): karbenitsilliin, tikartsilliin, karindatsilliin, karfetsilliin, flumitsilliin;
kombineeritud: tikartsilliin + klavulaanhape. - III. Põlvkond (ureidopenitsilliinid): aslotsilliin, piperatsilliin, metslotsilliin, apaltsilliin.
kombineeritud: piperatsilliin + tasobaktaam. - IV. Põlvkond (amidinopenitsilliinid): metsillinaam, pivamdinotsilliin, atsidotsilliin, amidinonilliin, bakamdinotsilliin.
- I. Põlvkond:
Bensüülpenitsilliin on penitsilliini rühma looduslik antibiootikum. Happekindel, hävitab beetalaktamaas (penitsillinaas). Seda kasutatakse naatriumi-, kaaliumi- ja novokaiinisoolade kujul. Bensüülpenitsilliinil on antibakteriaalne ja bakteritsiidne toime. Rikkub rakuseina peptidoglükaani sünteesi ja põhjustab mikroorganismide lüüsi. Aktiivne grampositiivsete bakterite vastu (Staphylococcus spp. tüved, mis ei moodusta penitsillinaasi, Streptococcus spp., sh Streptococcus pneumoniae), Corynebacterium diphtheriae, anaeroobseid eoseid moodustavaid vardaid, siberi katku pulgakesi, Actinomyces samuti cocci-, asegative spp. (Neisseria meningitidis, Neisseria gonorrhoeae), Treponema spp., Spirochaetaspp. Ebaefektiivne enamiku gramnegatiivsete bakterite, riketsia, viiruste, algloomade, seente vastu.
Bensüülpenitsilliini naatriumi- ja kaaliumisoolade / m manustamisel saavutatakse C max veres 30–60 minuti pärast, 3–4 tunni pärast leitakse verest antibiootikumi jälgi. Bensüülpenitsilliini novokaiinisool imendub aeglaselt ja sellel on pikaajaline toime; pärast ühekordset süstimist suspensioonina püsib penitsilliini terapeutiline kontsentratsioon veres kuni 12 tundi Seondumine verevalkudega on 60%. See tungib hästi elunditesse, kudedesse ja bioloogilistesse vedelikesse, välja arvatud tserebrospinaalvedelik, eesnääre. Põletikuga ajukelme läbib BBB-d. Eritub neerude kaudu glomerulaarfiltratsiooni (ligikaudu 10%) ja tubulaarsekretsiooni (90%) kaudu muutumatul kujul.
Selleks kasutatakse bensüülpenitsilliini bakteriaalsed infektsioonid tundlike patogeenide põhjustatud: kopsupõletik, pleura empüeem, KOK; septiline endokardiit (äge ja alaäge), haavainfektsioon, mädased infektsioonid nahk, pehmed koed ja limaskestad (sealhulgas erüsiipel, impetiigo, sekundaarselt nakatunud dermatoosid), mädane pleuriit, peritoniit, sepsis, osteomüeliit, ENT organite infektsioonid (tonsilliit), meningiit, difteeria, gaasigangreen, sarlakid, gonorröa, leptospiroos süüfilis, siberi katk, kopsude aktinomükoos, kuse- ja sapiteede infektsioonid, mädapõletiku ravi põletikulised haigused sünnitusabi ja günekoloogia praktikas.
Kasutamise vastunäidustused on ülitundlikkus, sh. teistele penitsilliinidele; epilepsia, hüperkaleemia, arütmia (kaaliumsoola puhul).
Kõrvaltoimetest on anafülaktilise šoki tekkimine, urtikaaria, Quincke turse, palavik / külmavärinad, peavalu, artralgia, eosinofiilia, interstitsiaalne nefriit, bronhospasm, nahalööbed.
Penitsilliinid, prolongeeritud ja poolsünteetilised
Bensüülpenitsilliini või depopenitsilliinide pikaajalised vormid: bitsilliin-1 (bensatiini bensüülpenitsilliin), samuti nendel põhinevad kombineeritud ravimid - bitsilliin-3 (bensatiinbensüülpenitsilliin + bensüülpenitsilliini naatrium + bensüülpenitsilliin novokaiinisool), bitsilliin-bensüülpenitsilliin-5 (bensüülbensüülpenitsilliin + 5) novokaiinisool)) on suspensioonid, mida saab manustada ainult intramuskulaarselt. Need imenduvad süstekohast aeglaselt, luues depoo lihaskoe. See võimaldab teil säilitada antibiootikumi kontsentratsiooni veres märkimisväärse aja jooksul ja seega vähendada sagedust ravimite manustamine. Kõiki bensüülpenitsilliini sooli kasutatakse parenteraalselt, tk. need hävivad mao happelises keskkonnas.
1957. aastal eraldati looduslikest penitsilliinidest 6-aminopenitsillaanhape ja selle baasil alustati poolsünteetiliste ravimite väljatöötamist, mida saadakse keemilise modifitseerimise teel, sidudes 6-aminopenitsillaanhappe molekulile erinevaid radikaale. Poolsünteetilistel penitsilliinidel on järgmised omadused: resistentsed penitsillinaaside (beeta-laktamaaside) toimele; happekindel, efektiivne suukaudsel manustamisel; neil on lai toimespekter.
Isoksasolüülpenitsilliine esindab peamiselt oksatsilliin. Ravimi toimespekter on kitsas, valdavalt mõjub grampositiivsele mikrofloorale. Oksatsilliin on resistentne beeta-laktamaasi toimele ja on stafülokoki (MSSA) kopsupõletiku valikravim. Oksatsilliini peamine kliiniline tähtsus on ravi stafülokokkinfektsioonid põhjustatud penitsilliiniresistentsetest tüvedest Staphylococcus aureus. Tuleb meeles pidada, et oksatsilliini ja metitsilliini suhtes resistentsed S.aureus tüved on haiglates tavalised (metitsilliini, esimese penitsilliiniresistentse penitsilliini, tootmine on lõpetatud). Neid tuntakse MRSA-na – Staphylococcus aureus aureuse metitsilliiniresistentsete tüvedena (metitsilliiniresistentsed S.aureus, MRSA). Oksatsilliini/metitsilliini suhtes resistentsed haigla- ja kogukonnas omandatud S.aureuse tüved on tavaliselt multiresistentsed – nad on resistentsed kõikide teiste beetalaktaamide ja sageli ka makroliidide, aminoglükosiidide ja fluorokinoloonide suhtes.
Naftsilliin on veidi aktiivsem kui oksatsilliin ja teised penitsillinaasi suhtes resistentsed ravimid. Naftsilliin tungib läbi BBB (selle kontsentratsioon tserebrospinaalvedelikus on stafülokoki meningiidi raviks piisav), eritub peamiselt sapiga (maksimaalne kontsentratsioon sapis on palju kõrgem kui seerumis), vähemal määral - neerude kaudu. Võib kasutada suukaudselt ja parenteraalselt.
Nüüd loetleme peamised farmakokineetilised erinevused isoksasoolpenitsilliinide ja bensüülpenitsilliini vahel:
- kiire, kuid mitte täielik (30-50%) imendumine seedetraktist. Neid antibiootikume võite kasutada nii parenteraalselt (in / m, in / in) kui ka sees, kuid 1-1,5 tundi enne sööki, sest. neil on madal vastupidavus vesinikkloriidhappele;
- kõrge plasmaalbumiiniga seondumise määr (90–95%) ja hemodialüüsi ajal isoksasolpenitsilliinide kehast eemaldamise võimatus;
- mitte ainult neerude, vaid ka maksa kaudu, kerge neerupuudulikkuse korral ei ole vaja annustamisskeemi kohandada.
Aminopenitsilliinid on esimese põlvkonna poolsünteetilised penitsilliinid, millel on lai toimespekter ja kõrge tundlikkus penitsillinaaside suhtes. Amoksitsilliinil on ampitsilliiniga võrreldes palju suurem suukaudne biosaadavus, mis võimaldab teil luua rohkem kõrged kontsentratsioonid ravim kudedesse (sh kopsudesse). Lisaks on amoksitsilliinil pikem poolväärtusaeg, mis võimaldab seda välja kirjutada 3 korda päevas, mitte 4, nagu ampitsilliinil. See muudab amoksitsilliini määramise eelistatavamaks kui ampitsilliini. Aminopenitsilliinid on laia toimespektriga antibiootikumid. Neid kõiki hävitavad nii grampositiivsete kui gramnegatiivsete bakterite beetalaktamaasid. Kliinilises praktikas kasutatakse laialdaselt amoksitsilliini ja ampitsilliini. Gram-positiivsete bakterite osas on ampitsilliin, nagu kõik poolsünteetilised penitsilliinid, aktiivsuselt madalam kui bensüülpenitsilliinil, kuid parem kui oksatsilliin.
Aminopenitsilliinide peamised omadused
Ampitsilliinil ja amoksitsilliinil on sarnane toimespekter. Võrreldes looduslike penitsilliinidega laieneb ampitsilliini ja amoksitsilliini antimikroobne toime tundlikele enterobakterite tüvedele, Escherichia coli, Proteus mirabilis, Salmonella spp., Shigella spp., Haemophilus influenzae; paremad looduslikud penitsilliinid toimivad Listeria monocytogenes'e ja tundlike enterokokkide vastu. Kõigist suukaudsetest beetalaktaamidest on amoksitsilliinil kõrgeim aktiivsus Streptococcus pneumoniae vastu, mis on resistentne looduslike penitsilliinide suhtes. Ampitsilliin on ebaefektiivne Staphylococcus spp. penitsillinaasi moodustavate tüvede, kõigi Pseudomonas aeruginosa tüvede, enamiku Enterobacter spp. tüvede, Proteus vulgaris (indoolpositiivne) tüvede vastu. Toodetakse kombineeritud preparaate, näiteks ampiokse (ampitsilliin + oksatsilliin). Ampitsilliini või bensüülpenitsilliini kombineerimine oksatsilliiniga on ratsionaalne, kuna. oksatsilliin on penitsillinaasi suhtes resistentne ja selle kombinatsiooni toimespekter muutub laiemaks. Erinevus amoksitsilliini (mis on üks juhtivaid suukaudseid antibiootikume) ja ampitsilliini vahel seisneb selle farmakokineetilises profiilis: suukaudsel manustamisel imendub amoksitsilliin soolestikus kiiremini ja paremini (75–90%) kui ampitsilliin (35–50%), biosaadavus ei sõltu toidust. Amoksitsilliin tungib paremini osadesse kudedesse, sh. bronhopulmonaarsesse süsteemi, kus selle kontsentratsioon on 2 korda kõrgem kui kontsentratsioon veres.
Kõige olulisemad erinevused aminopenitsilliinide ja bensüülpenitsilliinide farmakokineetilistes parameetrites:
- sees kohtumise võimalus;
- kerge seondumine plasmavalkudega - 80% aminopenitsilliinidest jääb verre vabal kujul - ja hea tungimine kudedesse ja kehavedelikesse (meningiidi korral võivad kontsentratsioonid tserebrospinaalvedelikus olla 70-95% vere kontsentratsioonist);
- kombineeritud ravimite määramise sagedus - 2-3 korda päevas.
Peamised aminopenitsilliinide määramise näidustused on ülemiste hingamisteede ja ENT organite infektsioonid, neerude ja kuseteede infektsioonid, seedetrakti infektsioonid, likvideerimine Helicobacter pylori(amoksitsilliin), meningiit. Aminopenitsilliinide soovimatu toime tunnuseks on "ampitsilliini" lööbe tekkimine, mis on mitteallergilise iseloomuga makulopapulaarne lööve, mis kaob ravimi kasutamise katkestamisel kiiresti. Üks aminopenitsilliinide määramise vastunäidustusi on nakkuslik mononukleoos.
Antipseudomonaalsete penitsilliinide hulka kuuluvad karboksüpenitsilliinid (karbenitsilliin, tikartsilliin) ja ureidopenitsilliinid (aslotsilliin, piperatsilliin). Karboksüpenitsilliinid ja ureidopenitsilliinid on oma toimespektri poolest sarnased aminopenitsilliinidega, kuid neil on väiksem aktiivsus grampositiivsete kokkide vastu, kuigi nende toime gramnegatiivsetele vardadele, sealhulgas Pseudomonas aeruginosale, on parem. See võimaldas neid pidada pseudomonasevastasteks ravimiteks. Pseudomonas aeruginosa vastase toime osas on nende rühmade preparaadid järjestatud järgmises aktiivsuse vähenemise järjekorras: aslotsilliin = piperatsilliin > tikartsilliin > karbenitsilliin. Sel juhul on eelistatav kasutada kaitstud karboksü- ja ureidopenitsilliini, kuna resistentsus monoravimitele on kõrge.
Inhibiitoriga kaitstud penitsilliinid
Karboksüpenitsilliinid on antibiootikumid, mille antimikroobne toime on sarnane aminopenitsilliinidele. Karbenitsilliin on esimene antipseudomonaalne penitsilliin, mille aktiivsus on teistest antipseudomonaalsetest penitsilliinidest madalam. Karboksüpenitsilliinid mõjutavad Pseudomonas aeruginosa (Pseudomonas aeruginosa) ja indoolpositiivseid Proteus liike (Proteus spp.), mis on resistentsed ampitsilliini ja teiste aminopenitsilliinide suhtes. Kliiniline tähtsus karboksüpenitsilliinide sisaldust vähendatakse. Kuigi neil on lai toimespekter, on nad inaktiivsed suure osa Staphylococcus aureus'e, Enterococcus faecalis'e, Klebsiella spp., Listeria monocytogenes'e tüvede vastu ega läbi peaaegu vere-aju barjääri. Kohtumiste arv - 4 korda päevas. Mikroorganismide sekundaarne resistentsus areneb kiiresti. hulgas kõrvaltoimed ravimit saab eraldada allergilised reaktsioonid, lokaalne ärritav toime, trombotsüütide agregatsiooni pärssimine, mõnikord trombotsütopeenia, kahjustus elektrolüütide tasakaalu: hüpernatreemia, hüpokaleemia (1,0 g ravimit sisaldab 5,4 mmol naatriumi), neurotoksilisus on suurem kui teistel penitsilliinidel.
Ureidopenitsilliinid on ka antipseudomonaalsed antibiootikumid, nende toimespekter langeb kokku karboksüpenitsilliinidega. Selle rühma kõige aktiivsem ravim on piperatsilliin. Selle rühma ravimitest säilitab meditsiinipraktikas oma tähtsuse ainult aslotsilliin. Ureidopenitsilliinid on P.aeruginosa vastu aktiivsemad kui karboksüpenitsilliinid. Neid kasutatakse ka Klebsiella spp. põhjustatud infektsioonide raviks. Kõik antipseudomonaalsed penitsilliinid hävitatakse beetalaktamaaside toimel. Ureidopenitsilliinide farmakokineetilised omadused:
- sisestage ainult parenteraalselt (in / m ja / in);
- eritumisel osalevad mitte ainult neerud, vaid ka maks;
- kasutamise sagedus - 3 korda päevas;
- bakterite sekundaarne resistentsus areneb kiiresti.
Penitsilliinidel ja teistel beetalaktaamantibiootikumidel on kõrge antimikroobne toime, kuid paljudel neist võib tekkida mikroobide resistentsus. See resistentsus on tingitud mikroorganismide võimest toota spetsiifilisi ensüüme - beetalaktamaase (penitsillinaase), mis hävitavad (hüdrolüüsivad) penitsilliinide beeta-laktaamtsüklit, mis jätab nad ilma antibakteriaalsest toimest ja põhjustab resistentsete mikroorganismitüvede arengut. . Mõned poolsünteetilised penitsilliinid on beetalaktamaaside toime suhtes resistentsed. Lisaks on omandatud resistentsuse ületamiseks välja töötatud ühendeid, mis võivad nende ensüümide aktiivsust pöördumatult pärssida, nn. beeta-laktamaasi inhibiitorid. Neid kasutatakse inhibiitoritega kaitstud penitsilliinide loomisel. Beeta-laktamaasi inhibiitorid, nagu penitsilliinid, on beeta-laktaamühendid, kuid neil endal on minimaalne antibakteriaalne toime. Need ained seonduvad pöördumatult beetalaktamaasidega ja inaktiveerivad need ensüümid, kaitstes seeläbi beetalaktaamantibiootikume hüdrolüüsi eest. Beeta-laktamaasi inhibiitorid on kõige aktiivsemad plasmiidsete geenide poolt kodeeritud beeta-laktamaaside suhtes.
Inhibiitoriga kaitstud penitsilliinid on kombinatsioon penitsilliini antibiootikumist spetsiifilise beetalaktamaasi inhibiitoriga (klavulaanhape, sulbaktaam, tasobaktaam). Beetalaktamaasi inhibiitoreid ei kasutata üksi, vaid neid kasutatakse koos beetalaktaamidega. See kombinatsioon võimaldab teil suurendada antibiootikumi resistentsust ja selle aktiivsust mikroorganismide suhtes, mis toodavad neid ensüüme (beeta-laktamaas): S.aureus, H.influenzae, M.catarrhalis, N.gonorrhoeae, E.coli, Klebsiella spp., Proteus spp., anaeroobid, sh. B.fragilis. Selle tulemusena muutuvad penitsilliinide suhtes resistentsed mikroorganismide tüved kombineeritud ravimi suhtes tundlikuks. Inhibiitoriga kaitstud beetalaktaamide antibakteriaalse toime spekter vastab nende koostises sisalduvate penitsilliinide spektrile, erineb ainult omandatud resistentsuse tase.
Inhibiitoriga kaitstud penitsilliinid on kasutusel erineva lokaliseerimisega infektsioonide raviks ja perioperatiivseks profülaktikaks kõhukirurgia puhul. Inhibiitoriga kaitstud penitsilliinide hulka kuuluvad amoksitsilliin/klavulanaat, ampitsilliin/sulbaktaam, amoksitsilliin/sulbaktaam, piperatsilliin/tasobaktaam, tikartsilliin/klavulanaat. Tikartsilliinil/klavulanaadil on antipseudomonaalne toime ja see on aktiivne S. maltophilia vastu.
Sulbaktaamil on oma antibakteriaalne toime Neisseriaceae perekonna gramnegatiivsete kokkide ja Acinetobacter perekonna mittefermenteerivate bakterite vastu.
Millal määratakse penitsilliinid?
Penitsilliinid kasutatakse peamiselt ülemiste hingamisteede infektsioonide, tonsilliidi, sarlakid, keskkõrvapõletiku, sepsise, süüfilise, gonorröa, seedetrakti infektsioonide, kuseteede infektsioonide jne ravis. Tuleb meeles pidada, et ebapiisavate annuste kasutamine penitsilliinid (nagu ka teised antibiootikumid) või liiga varane ravi lõpetamine võib viia resistentsete mikroorganismitüvede (eriti looduslike penitsilliinide) tekkeni. Resistentsuse ilmnemisel tuleb jätkata antibiootikumravi.
Penitsilliinidel on antibiootikumide seas madalaim toksilisus ja lai valik ravitoimeid (eriti looduslikud). Penitsilliinid on tavalisemad kui teised ravimid farmakoloogilised rühmad, on põhjuseks ravimite allergia. Penitsilliinide kasutamisel on võimalikud kahte tüüpi allergilised reaktsioonid - kohene ja hiline (hiline). Arvatakse, et allergiline reaktsioon penitsilliinidele on seotud peamiselt nende ainevahetuse vaheproduktiga - penitsilliini rühmaga. Seda nimetatakse peamiseks antigeenseks determinandiks ja see moodustub beeta-laktaamitsükli purunemisel. Penitsilliinide väikesed antigeensed determinandid hõlmavad eelkõige penitsilliinide muutumatuid molekule, bensüülpenitsiloaati. Need moodustuvad in vivo, kuid määratakse ka manustamiseks valmistatud penitsilliinilahustes. Arvatakse, et varased allergilised reaktsioonid penitsilliinidele on vahendatud peamiselt IgE antikehade poolt väikeste antigeensete determinantide, hilinenud ja hilise (urtikaaria) suhtes – tavaliselt suure antigeense determinandi vastaste IgE antikehade kaudu.
Ülitundlikkusreaktsioonid on põhjustatud antikehade moodustumisest organismis ja tekivad tavaliselt mõni päev pärast penitsilliini kasutamise algust (aeg võib varieeruda mõnest minutist mitme nädalani). Mõnel juhul ilmnevad allergilised reaktsioonid anafülaktilise šoki, nahalööbe, dermatiidi ja palaviku kujul. Raskematel juhtudel väljenduvad need reaktsioonid limaskestade turse, artriidi, artralgia, neerukahjustuse ja muude häiretena. Raske allergiline reaktsioon on absoluutne vastunäidustus penitsilliinide kasutuselevõtule tulevikus. Patsiendile tuleb selgitada, et isegi mitte suur hulk toiduga või nahatesti käigus organismi sattunud penitsilliin võib olla talle surmav.
Kõikidele penitsilliinidele on iseloomulik ristsensibiliseerimine ja ristallergilised reaktsioonid.
Penitsilliinid võivad põhjustada mitmesuguseid mitteallergilise iseloomuga kõrvaltoimeid ja toksilisi toimeid. Nende hulka kuuluvad: suukaudsel manustamisel - ärritav toime, sh. glossiit, stomatiit, iiveldus, kõhulahtisus; / m sissejuhatusega - valu, infiltraat, lihaste aseptiline nekroos; koos / sissejuhatuses - flebiit, tromboflebiit. Võimalik tõus refleksi erutuvus KNS. Suurte annuste kasutamisel võivad tekkida neurotoksilised toimed: hallutsinatsioonid, deliirium, vererõhu reguleerimise häired, krambid. Krambid on tõenäolisemad patsientidel, kes saavad suuri penitsilliini annuseid ja/või raske maksakahjustusega patsientidel. Raskete neurotoksiliste reaktsioonide ohu tõttu ei saa penitsilliinid manustada endolumbaalselt (erandiks on bensüülpenitsilliini naatriumsool, mida manustatakse äärmiselt ettevaatlikult, vastavalt elulistele näidustustele). Penitsilliinide ravis superinfektsiooni, suuõõne kandidoosi, tupe, soole düsbakterioos. Penitsilliinid (sagedamini ampitsilliin) võivad põhjustada antibiootikumidega seotud kõhulahtisust.
Ampitsilliini kasutamine põhjustab "ampitsilliini" lööbe ilmnemist. See kõrvaltoime esineb sagedamini lümfadenopaatia ja viirusnakkustega lastel ampitsilliini suurte annuste 5.–10. päeval.
Oksatsilliini kasutamisel on võimalik hematuria, proteinuuria ja interstitsiaalne nefriit.
Antipseudomonaalsete penitsilliinide (karboksüpenitsilliinid, ureido-penitsilliinid) kasutamisega võivad kaasneda allergilised reaktsioonid, neurotoksilisuse sümptomid, äge interstitsiaalne nefriit, düsbakterioos, trombotsütopeenia, neutropeenia, leukopeenia, eosinofiilia. Karbenitsilliini kasutamisel - hemorraagiline sündroom.
Klavulaanhapet sisaldavad kombineeritud ravimid võivad põhjustada ägedat maksakahjustust. Vastavalt FDA (Food and Drug Administration) üldtunnustatud soovitustele, mis määravad kindlaks ravimite kasutamise võimaluse raseduse ajal, kuuluvad penitsilliini rühma ravimid nende toime poolest lootele FDA B-kategooriasse (sigimise uuring). loomadel ei näidanud ravimite kahjulikku mõju lootele, kuid piisav ja range kontrollitud uuringud ei tehta rasedatele).
Ettevaatlik tuleb olla Pseudomonas aeruginosa vastu aktiivsete penitsilliinide kombineerimisel antikoagulantide ja trombotsüütidevastaste ainetega ( võimalik risk suurenenud verejooks). Penitsilliinide kombineerimine trombolüütikumidega ei ole soovitatav. Sulfoonamiididega kombineerimisel võib bakteritsiidne toime nõrgeneda. Suukaudsed penitsilliinid võivad enterohepaatilise östrogeeni tsirkulatsiooni halvenemise tõttu vähendada suukaudsete rasestumisvastaste vahendite efektiivsust. Ampitsilliini ja allopurinooli kombinatsioon suurendab nahalööbe tekkimise tõenäosust. bensüülpenitsilliini kaaliumsoola suurte annuste kasutamine koos kaaliumi säästvate diureetikumide, kaaliumipreparaatide või AKE inhibiitorid suurendab hüperkaleemia riski. Penitsilliinid on farmatseutiliselt kokkusobimatud aminoglükosiididega. Kuna antibiootikumide pikaajalisel suukaudsel manustamisel võib pärssida vitamiine B 1, B 6, B 12, PP tootvat soolestiku mikrofloorat, on hüpovitaminoosi vältimiseks soovitatav patsientidele määrata B-rühma vitamiine.
Antibiootikumid (a / b) - ained, mis eksisteerivad looduses või on sünteesitud inimese poolt looduslikust toorainest ja pärsivad kasvu patogeensed bakterid mis ründavad keha. Antibiootikume kasutatakse onkoloogias ka vähivastaste ravimitena.
Penitsilliini ja selle omaduste avastamine
Paljud haigused tundusid enne antibiootikumide avastamist ravimatud, arstid ja teadlased üle maailma soovisid leida ainet, mis aitaks patogeensetest mikroobidest jagu ilma inimorganismi kahjustamata. Inimesed surid bakteritega nakatunud haavadesse, sepsise, kopsupõletiku, tuberkuloosi, gonorröa ja teiste sama ohtlike haiguste tõttu.
 Pöördepunktiks meditsiini ajaloos peetakse 1928. aastat – penitsilliini avastamise aastat. Selle avastuse tõttu on päästetud miljoneid elusid Sir Alexander Fleming, kelle nimi on tuntud kogu maailmas. Kogemata kasvanud hallitusseened liigist Penicillium notatum on sööde Flemingi laboris ja teadlase enda vaatlus andis võimaluse nakkushaigustest jagu saada.
Pöördepunktiks meditsiini ajaloos peetakse 1928. aastat – penitsilliini avastamise aastat. Selle avastuse tõttu on päästetud miljoneid elusid Sir Alexander Fleming, kelle nimi on tuntud kogu maailmas. Kogemata kasvanud hallitusseened liigist Penicillium notatum on sööde Flemingi laboris ja teadlase enda vaatlus andis võimaluse nakkushaigustest jagu saada.
Pärast penitsilliini avastamist oli teadlastel üks ülesanne - see aine isoleerida puhtal kujul. Asi osutus mitte lihtsaks, kuid 20. sajandi 40. aastate alguses õnnestus kahel teadlasel, Howard Floreyl ja Ernst Cheyne'il sünteesida antibakteriaalsete omadustega ravim.
Penitsilliinide omadused
Penitsilliini rühma antibiootikumid pärsivad selliste mikroorganismide kasvu ja arengut nagu:

See on vaid väike loetelu bakteritest, mille elutähtsat aktiivsust pärsivad penitsilliin ja selle perekonna ravimid.

Penitsilliinide klassifikatsioon ja ravimite loetelu
Penitsilliinide perekonna keemilise valemi alus sisaldab beeta-laktaamtsüklit, seega klassifitseeritakse need beeta-laktaamantibiootikumideks.
Kuna penitsilliini on meditsiinis kasutatud enam kui 70 aastat, on mõnedel bakteritel tekkinud selle aine suhtes resistentsus beetalaktamaasi ensüümi näol.
Ensüümi toimemehhanism on beeta-laktaamitsükli afiinsus bakteriraku hüdrolüütilise ensüümi suhtes, mis hõlbustab nende seondumist ja selle tulemusena antibiootikumi inaktiveerimist.
Maks on peamine organ Inimkeha kes võtab transformatsioonist aktiivselt osa ravimid mehe poolt vastu võetud. Sellepärast see nii ongi oluline on kaitsta oma maksa alates negatiivne mõju pärast sunnitud antibiootikume või nende ajal koos ...
 peal Sel hetkel poolsünteetilisi antibiootikume kasutatakse suuremal määral: võetakse alus keemiline valem looduslik antibiootikum ja läbib kasulikke modifikatsioone. Tänu sellele on inimkond endiselt võimeline seista vastu bakteritele, mis igal aastal arendavad välja oma antibiootikumiresistentsuse mehhanismid.
peal Sel hetkel poolsünteetilisi antibiootikume kasutatakse suuremal määral: võetakse alus keemiline valem looduslik antibiootikum ja läbib kasulikke modifikatsioone. Tänu sellele on inimkond endiselt võimeline seista vastu bakteritele, mis igal aastal arendavad välja oma antibiootikumiresistentsuse mehhanismid.
Kehtivad föderaalsed ravimite kasutamise juhised näevad ette järgmine klassifikatsioon penitsilliinid:


Vaatleme veidi lähemalt iga antibiootikumiklassi juures ja vaatame, millistel juhtudel neid kasutatakse.
Looduslikud antibiootikumid lühitoimelised
Looduslikel antibiootikumidel ei ole beetalaktamaasi inhibiitoreid, seega ei kasutata neid kunagi stafülokoki infektsioonide vastu.
 Bensüülpenitsilliin on aktiivne siberi katku ravis, lobaarne kopsupõletik, pleuriit, bronhiit, sepsis, peritoniit, meningiit (täiskasvanutel ja üle 2-aastastel lastel), haigused Urogenitaalsüsteem, ENT haigused, haavainfektsioonid ja nahainfektsioonid.
Bensüülpenitsilliin on aktiivne siberi katku ravis, lobaarne kopsupõletik, pleuriit, bronhiit, sepsis, peritoniit, meningiit (täiskasvanutel ja üle 2-aastastel lastel), haigused Urogenitaalsüsteem, ENT haigused, haavainfektsioonid ja nahainfektsioonid.
Kasutamise vastunäidustused ja piirangud: allergia penitsilliinile, heinapalavik, bronhiaalastma, arütmia, neerufunktsiooni kahjustus.
Kõrvaltoimed: kõigi penitsilliinirühma antibiootikumide puhul on peamiseks kõrvaltoimeks allergiline reaktsioon anafülaktilise šoki, urtikaaria, Quincke turse, hüpertermia, nefriidi, nahalööbe kujul. Võimalikud tõrked südametöös. Suurte annuste kasutuselevõtuga - krambid (lastel).
Looduslikud pika toimeajaga antibiootikumid
Bensüülpenitsilliini bensatiini kasutatakse süüfilise, mandlipõletiku, sarlaki, haavapõletike korral. Kasutatakse operatsioonijärgsete tüsistuste vältimiseks.
 Vastunäidustused: kalduvus allergilistele reaktsioonidele penitsilliinile, bronhiaalastma, heinapalavik. Kõrvaltoimed: allergiline reaktsioon, aneemia, leukopeenia ja trombotsütopeenia, peavalu, abstsess süstekohas.
Vastunäidustused: kalduvus allergilistele reaktsioonidele penitsilliinile, bronhiaalastma, heinapalavik. Kõrvaltoimed: allergiline reaktsioon, aneemia, leukopeenia ja trombotsütopeenia, peavalu, abstsess süstekohas.
Bensüülpenitsilliini prokaiini kasutatakse ägedate hingamisteede põletikuliste haiguste, septilise endokardiidi, meningiidi, osteomüeliidi, peritoniidi, urogenitaal- ja sapiteede põletike, haavainfektsioonide, dermatooside, silmahaiguste ravis. Kasutatakse reuma ja erüsiipe ägenemiste korral.
Vastunäidustused: ülitundlikkus penitsilliini ja prokaiini suhtes. Kõrvalmõju: allergiline reaktsioon, iiveldus, krambid.
Antistafülokoki ravimid
Oksatsilliini peetakse selle antibiootikumide rühma peamiseks esindajaks. Toimespekter on sarnane bensüülpenitsilliiniga, kuid erinevalt viimasest on see aine võimeline hävitama stafülokokkinfektsioone.
Vastunäidustused: allergia penitsilliini suhtes. Kõrvaltoimed: urtikaaria, nahalööbed. Harva - turse, anafülaktiline šokk.
Tagasiside meie lugejalt - Maria Ostapova
Lugesin hiljuti artiklit, kus öeldi, et iga haigust tuleb hakata ravima maksa puhastamisega. Ja räägiti "Leviron Duo" vahendist maksa kaitsmiseks ja puhastamiseks. Abiga seda ravimit te ei saa mitte ainult kaitsta oma maksa antibiootikumide võtmise negatiivsete mõjude eest, vaid ka seda taastada.
Ma polnud harjunud mingit teavet usaldama, kuid otsustasin kontrollida ja tellisin paki. Hakkasin seda võtma ja märkasin, et mul on jõudu, muutusin energilisemaks, kibedus suust kadus, ebamugavustunne kõhupiirkonnas paranes jume. Proovige ja sina ja kui kedagi huvitab, siis allpool on link artiklile.
Seedehäired, palavik, iiveldus, oksendamine, kollatõbi, hematuuria (lastel).
Laia toimespektriga antibiootikumid
Ampitsilliini kui toimeainet kasutatakse paljudes antibiootikumides. Kasutatakse nakkushaiguste raviks seedeelundkond, ägedad infektsioonid hingamisteede ja kuseteede, meningiit, endokardiit, klamüüdiainfektsioonid.
 Ampitsilliini sisaldavate ravimite loetelu: Ampitsilliini trihüdraat, Ampitsilliini naatriumsool, Ampicillin-AKOS, Ampicillin AMP-Forte, Ampicillin-Inotek jt.
Ampitsilliini sisaldavate ravimite loetelu: Ampitsilliini trihüdraat, Ampitsilliini naatriumsool, Ampicillin-AKOS, Ampicillin AMP-Forte, Ampicillin-Inotek jt.
Amoksitsilliin on ampitsilliini täiustatud derivaat. See on juhtiv antibiootikum, mida võetakse suu kaudu, st suu kaudu. Kasutatakse ägedate hingamisteede haigused, meningokoki infektsioonid, põletikulised protsessid seedetrakt, Lyme'i tõbi. Kasutatakse siberi katku ennetamiseks lastel ja rasedatel.
Amoksitsilliini sisaldavate ravimite loetelu: Amoxisar, Amoxicillin Sandoz, Amoxicillin-ratiopharm, Amoxicillin DS jne.
Selle a/b rühma vastunäidustused: ülitundlikkus, rasedus, maksafunktsiooni kahjustus, mononukleoos. Ampitsilliin on vastunäidustatud alla 1 kuu vanustele lastele.
Kõrvaltoimed: düspeptilised häired, düsbakterioos, kandidoos, allergiad, kesknärvisüsteemi häired, superinfektsioon.
Antipseudomonaalsed ravimid
Karboksüpenitsilliinid sisaldavad toimeaine- karbenitsilliin. AT sel juhul Ravimi nimi on sama, mis toimeaine. Seda kasutatakse Pseudomonas aeruginosa põhjustatud haiguste raviks. Praegu seda meditsiinis praktiliselt ei kasutata aktiivsemate ravimite kättesaadavuse tõttu.
Ureidopenitsilliinide hulka kuuluvad: metsotsilliin, piperatsilliin, aslotsilliin. Vastunäidustused: ülitundlikkus penitsilliinile, rasedus.
Kõrvalmõju: söömishäired, iiveldus, oksendamine, urtikaaria. Võimalik ravimipalavik, peavalu, neerufunktsiooni kahjustus, superinfektsioon.
Penitsilliini antibiootikumide kasutamise tunnused lastel.
Antibiootikumide kasutamine pediaatrilises ravis on alati ette nähtud suurenenud tähelepanu, kuna lapse keha pole veel täielikult moodustunud ja paljud organsüsteemid ei tööta täisjõud. Seetõttu on ravimi valik vastsündinutele ja lastele noorem vanus arstid peaksid vastutama.
 Vastsündinutel kasutatakse penitsilliini sepsise ja toksiliste haiguste korral. Esimestel eluaastatel lastel kasutatakse seda kopsupõletiku, kõrvapõletiku, pleuriidi, meningiidi raviks.
Vastsündinutel kasutatakse penitsilliini sepsise ja toksiliste haiguste korral. Esimestel eluaastatel lastel kasutatakse seda kopsupõletiku, kõrvapõletiku, pleuriidi, meningiidi raviks.
ARVI, tonsilliidi, sinusiidi, bronhiidi, tsüstiidi korral määratakse lastele kõige sagedamini Amoxicillin, Flemoxin, Amoxiclav, Augmentin. Neid antibiootikume peetakse tõhusamaks ja lapse kehale vähem toksilisteks.
Düsbakterioos on üks antibiootikumravi tüsistusi, kuna kasulik mikrofloora lapsed surevad koos patogeensete bakteritega. Seetõttu tuleb antibiootikumravi kombineerida probiootikumide kasutamisega. Harv kõrvaltoime on allergiline reaktsioon penitsilliinile lööbe kujul.
Vastsündinutel ja väikelastel ei ole neerude eritusfunktsioon piisavalt arenenud ning võimalik on penitsilliini kuhjumine organismi. Selle tagajärjeks on krampide teke.
Nüüd on meie elu ilma antibiootikumideta raske ette kujutada. Nende abiga on võimalik ravida paljusid inimkonda vaevavaid haigusi. Aga sa pead sellest aru saama sagedane kasutamine antibiootikumid ei ole mitte ainult kahjulikud inimkehale, vaid kasulikud ka bakteritele, mille vastu neid kasutatakse. Enne antibiootikumide kasutamist pidage alati nõu oma arstiga.
Teie keha püüab olla terve, aidake teda selles!
Kas teie ja teie pere haigestuvad väga sageli ja saate ravi ainult antibiootikumidega? Kas olete proovinud palju erinevaid ravimeid, kulutanud palju raha, vaeva ja aega, kuid tulemus on null? Tõenäoliselt ravite tagajärge, mitte põhjust.
Nõrk ja vähenenud immuunsus muudab meie keha DEFEKTIIVSEKS. See ei suuda vastu seista mitte ainult infektsioonidele, vaid ka patoloogilistele protsessidele, mis põhjustavad KASVAJAID JA VÄHI! Kui olete tuttav:
- sagedased hingamisteede külmetushaigused ja viirushaigused;
- ARVI pika ja raske kuluga;
- püsivad pustuloossed nahakahjustused;
- suurendama lümfisõlmed;
- seenhaigus küüned, nahk ja limaskestad (onühhomükoos, kandidoos);
- tuberkuloosi infektsioon mis tahes vormides ja ilmingutes;
- resistentne ravile ja pidevalt korduvad hingamisteede, ninakõrvalurgete, kuseteede haigused;
- halb haavade paranemine;
- üldine nõrkus, krooniline väsimus.
Peame kiiresti tegutsema! Seetõttu otsustasime avaldada eksklusiivne intervjuu koos Aleksander Mjasnikov milles see on jagatud penni meetod immuunsuse tugevdamine.
Antibakteriaalsed kemoterapeutilised ained hõlmavad järgmisi ravimirühmi:
• antibiootikumid;
• sünteetiline antibakteriaalsed ained;
• antisüüfilised ained;
• tuberkuloosivastased ravimid.
37.1. ANTIBIOOTIKUD
Antibiootikumid- Need on bioloogilist päritolu kemoterapeutilised ained, mis selektiivselt pärsivad mikroorganismide elutähtsat aktiivsust.
Antibiootikumide klassifitseerimisel kasutatakse erinevaid põhimõtteid.
Sõltuvalt saamise allikatest jagatakse antibiootikumid kahte rühma:
• looduslik (biosünteetiline), toodetud mikroorganismide ja madalamate seente poolt;
• poolsünteetiline, mis saadakse looduslike antibiootikumide struktuuri muutmisel.
Vastavalt keemilisele struktuurile eristatakse järgmisi antibiootikumide rühmi:
• β-laktaamantibiootikumid (penitsilliinid, tsefalosporiinid, karbapeneemid, monobaktaamid);
• makroliidid ja sarnased antibiootikumid;
• aminoglükosiidid;
• tetratsükliinid;
• polümüksiinid;
• polüeenid (seenevastased antibiootikumid);
• klooramfenikooli preparaadid (levomütsetiin *);
• glükopeptiidantibiootikumid;
• erinevate keemiliste rühmade antibiootikumid.
Antibiootikumide toime olemus (tüüp) võib olla bakteritsiidne (seened või algloomad, olenevalt patogeenist), mille all mõistetakse nakkustekitaja raku täielikku hävitamist, ja bakteriostaatiline (seene-, algloomarakk), mis avaldub. selle rakkude kasvu ja jagunemise peatumisega.
Antibiootikumide toime bakteritsiidne või bakteriostaatiline olemus mikrofloorale on suuresti määratud nende toimemehhanismi iseärasustega. Määras selle antimikroobne toime antibiootikumid arenevad peamiselt rikkumise tagajärjel:
• mikroorganismide rakuseina süntees;
• tsütoplasmaatilise membraani läbilaskvus mikroobirakk;
• intratsellulaarne valkude süntees mikroobirakus;
• RNA süntees mikroorganismides.
Kui võrrelda antibiootikumide olemust ja toimemehhanismi (tabel 37-1), siis on näha, et bakteritsiidse toime annavad peamiselt need antibiootikumid, mis rikuvad rakuseina sünteesi, muudavad tsütoplasma membraani läbilaskvust või rikuvad. RNA süntees mikroorganismides. Bakteriostaatiline toime on iseloomulik antibiootikumidele, mis häirivad rakusisest valkude sünteesi.
Tabel 37-1
Antibiootikumide antimikroobse toime mehhanism ja olemus
Toimemehhanism | Antibiootikumid | Antimikroobse toime domineeriv olemus |
Rakuseina sünteesi rikkumine | β-laktaamantibiootikumid | bakteritsiidne |
Glükopeptiidantibiootikumid | bakteritsiidne |
|
Tsükloseriin | bakteritsiidne |
|
Batsitratsiin | bakteritsiidne |
|
Tsütoplasmaatilise membraani läbilaskvuse rikkumine | Polümüksiinid | bakteritsiidne |
Polüeenantibiootikumid | bakteritsiidne |
|
Intratsellulaarse valgusünteesi rikkumine | Makroliidid | Bakteriostaatiline |
Tetratsükliinid | Bakteriostaatiline |
|
Linkosamiidid | Bakteriostaatiline |
|
Kloramfenikool | Bakteriostaatiline |
|
Aminoglükosiidid | bakteritsiidne |
|
RNA sünteesi rikkumine | Rifampitsiin | bakteritsiidne |
Antimikroobse toime spektri järgi võib antibiootikumid jagada laia toimespektriga (toimivad grampositiivsele ja gramnegatiivsele mikrofloorale: tetratsükliinid, klooramfenikool, aminoglükosiidid, tsefalosporiinid, poolsünteetilised penitsilliinid) ja suhteliselt kitsa toimespektriga ravimiteks. tegevust. Teise rühma ravimid jagunevad omakorda antibiootikumideks, mis toimivad peamiselt grampositiivsele mikrofloorale (biosünteetilised penitsilliinid, makroliidid) ja anti-
biootikumid, mis mõjutavad peamiselt gramnegatiivset mikrofloorat (polümüksiinid). Lisaks on olemas seene- ja kasvajavastased antibiootikumid.
Kõrval kliiniline rakendus eraldama peamised antibiootikumid, millega alustatakse ravi kuni neile haigust põhjustanud mikroorganismide tundlikkuse kindlaksmääramiseni ja reservantibiootikumid, mida kasutatakse mikroorganismide resistentsuse korral põhiantibiootikumide suhtes või talumatuse korral viimaste suhtes. .
Antibiootikumide kasutamise käigus võib nende suhtes tekkida mikroorganismide resistentsus (resistentsus), s.o. mikroorganismide võime paljuneda antibiootikumi terapeutilise annuse juuresolekul. Mikroorganismide resistentsus antibiootikumide suhtes võib olla loomulik ja omandatud.
Looduslikku resistentsust seostatakse antibiootikumi toime "sihtmärgi" puudumisega mikroorganismides või "sihtmärgi" kättesaamatusega, mis on tingitud rakuseina madalast läbilaskvusest, samuti antibiootikumi ensümaatilisest inaktiveerimisest. Kui bakterid on looduslikult resistentsed, on antibiootikumid kliiniliselt ebaefektiivsed.
Omandatud resistentsuse all mõistetakse üksikute bakteritüvede võimet jääda elujõuliseks selliste antibiootikumide kontsentratsioonide juures, mis pärsivad suuremat osa mikroobide populatsioonist. Omandatud resistentsus on seotud kas spontaansete mutatsioonidega bakteriraku genotüübis või plasmiidide ülekandmisega looduslikult resistentsetelt bakteritelt vastuvõtlikele liikidele.
Bakterite antibiootikumide suhtes resistentsuse tekitamiseks on teada järgmised biokeemilised mehhanismid:
• ravimite ensümaatiline inaktiveerimine;
• antibiootikumide "sihtmärgi" muutmine;
• aktiivne eritumine antibakteriaalsed ravimid mikroobirakust;
• bakteriraku seina läbilaskvuse vähenemine;
• metaboolse "šundi" moodustumine.
Mikroorganismide resistentsus antibiootikumide suhtes võib olla rühmaspetsiifiline, s.t. resistentsus mitte ainult kasutatava ravimi, vaid ka teiste samade ravimite suhtes keemiline rühm. Seda stabiilsust nimetatakse risttakistuseks.
Kemoterapeutiliste ainete kasutamise põhimõtete järgimine võib vähendada resistentsuse tõenäosust.
Hoolimata asjaolust, et antibiootikume iseloomustab toime kõrge selektiivsus, annavad nad mõningaid allergilisi ja mitteallergilisi kõrvaltoimeid.
β-laktaamantibiootikumid
β-laktaamantibiootikumid (penitsilliinid, tsefalosporiinid, karbapeneemid ja monobaktaamid) on ravimid, mille molekulis on β-laktaamtsükkel, mis on vajalik nende ühendite antimikroobse toime rakendamiseks. Kui β-laktaamtsükkel lõhustatakse bakteriaalsete ensüümide (β-laktamaaside) toimel, kaotavad antibiootikumid oma antibiootikumivõime.
Kõik β-laktaamantibiootikumid on bakteritsiidne toime, mis põhineb nende bakteriraku seina sünteesi pärssimisel. Selle rühma antibiootikumid häirivad peptidoglükaani, biopolümeeri, bakteriraku seina põhikomponendi sünteesi. Peptidoglükaan koosneb polüsahhariididest ja polüpeptiididest.
Polüsahhariidide koostis sisaldab aminosuhkruid - N-atsetüülglükoosamiini ja N-atsetüülmuraamhapet. Aminosuhkrud on seotud lühikeste peptiidahelatega. Rakuseina lõpliku jäikuse annavad ristsuunalised peptiidahelad, mis koosnevad viiest glütsiinijäägist (pentaglütsiini sillad). Peptiidoglükaani süntees toimub kolmes etapis:
• peptidoglükaani prekursorite (N-atsetüülmuramüülpentapeptiid ja N-atsetüülglükoosamiin) süntees tsütoplasmas, nende ülekandmine läbi tsütoplasmaatilise membraani batsitratsiini poolt inhibeeritud lipiidide transporteri osalusel;
• nende prekursorite lisamine kasvavasse polümeeriahelasse;
• ristsidemete moodustumine kahe külgneva ahela vahel ensüümi (peptidoglükaan-transpeptidaasi) poolt katalüüsitava transpeptideerimisreaktsiooni tulemusena.
Peptiidoglükaani lõhustamise protsessi katalüüsib ensüüm (mureiini hüdrolaas), mille aktiivsus normaalsetes tingimustes inhibeerib endogeenne inhibiitor.
β-laktaamantibiootikumid inhibeerivad:
• peptidoglükaan-transpeptidaas, mis põhjustab selle moodustumise häireid;
• endogeenne inhibiitor, mis viib mureiini hüdrolaasi aktiveerumiseni, mis lõhustab peptidoglükaani.
β-laktaamantibiootikumid on makroorganismile madala toksilisusega, kuna inimese rakumembraanid ei sisalda peptidoglükaani. Selle rühma antibiootikumid on tõhusad peamiselt pigem jagunevate kui puhkerakkude vastu, kuna aktiivse kasvu faasis olevates rakkudes toimub peptidoglükaani süntees kõige intensiivsemalt.
Penitsilliinid
Penitsilliinide struktuur põhineb 6-aminopenitsillaanhappel, heterotsüklilisel süsteemil, mis koosneb kahest kondenseerunud tsüklist: neljaliikmelisest β-laktaamist ja viieliikmelisest tiasolidiinist.
Penitsilliinid erinevad üksteisest 6-aminopenitsillaanhappe aminorühma atsüüljäägi struktuuri poolest.
Valmistamismeetodi järgi eraldatakse looduslikud (biosünteetilised) ja poolsünteetilised penitsilliinid.
looduslikud penitsilliinid
Looduslikud penitsilliinid – sünteesiprodukt mitmesugused perekonna seen Penicillium.
Looduslike penitsilliinide toimespekter hõlmab valdavalt grampositiivseid mikroorganisme:
• grampositiivsed kokid (streptokokid, pneumokokid; stafülokokid, mis ei tooda penitsillinaasi);
• grampositiivsed pulgad (difteeria, siberi katku, listeria tekitajad);
• anaeroobid (klostriidid);
• aktinomütseedid; sama hästi kui:
• gramnegatiivsed kookid (meningokokid ja gonokokid);
• spiroheedid (kahvatu treponema, leptospira, borrelia).
Looduslikke penitsilliine kasutatakse:
• tonsillofarüngiit (stenokardia);
• sarlakid;
• erüsiipel;
• bakteriaalne endokardiit;
• kopsupõletik;
• difteeria;
• meningiit;
• mädased infektsioonid;
• gaasi gangreen;
• aktinomükoos.
Selle rühma ravimid on valikvahendid süüfilise ravis ja reumaatiliste haiguste ägenemiste ennetamisel.
Kõik looduslikud penitsilliinid hävitatakse β-laktamaaside (penitsillinaaside) toimel, seetõttu ei saa neid kasutada stafülokoki infektsioonide raviks, kuna enamasti on põhjustajaks penitsillinaasi tootv staphylococcus aureus.
Eristama järgmised ravimid looduslikud penitsilliinid.
• Preparaadid parenteraalseks manustamiseks (happekindlad).
- lühike tegevus. Bensüülpenitsilliini naatriumi- ja kaaliumisoolad*.
Bensüülpenitsilliini prokaiin (bensüülpenitsilliini novokaiini sool *), bensatiinbensüülpenitsilliin (bitsilliin-1 *), bensatiinbensüülpenitsilliin + bensüülpenitsilliin prokaiin (bitsilliin-5 *).
• Enteraalseks manustamiseks mõeldud preparaadid (happekindlad). Fenoksümetüülpenitsilliin.
Bensüülpenitsilliini naatriumi ja kaaliumi soolad * - bensüülpenitsilliini hästi lahustuvad preparaadid. Need imenduvad kiiresti süsteemsesse vereringesse ja tekitavad vereplasmas kõrge kontsentratsiooni, mis võimaldab neid kasutada ägedate, raskete nakkusprotsesside korral. Kell intramuskulaarne süstimine ravimid kogunevad verre maksimaalsetes kogustes 30-60 minuti pärast ja elimineeruvad organismist peaaegu täielikult 3-4 tunni pärast, seega tuleb ravimite intramuskulaarset süstimist teha iga 3-4 tunni järel Raskete septiliste seisundite korral on ravimilahused manustatakse intravenoosselt. Bensüülpenitsilliini naatriumsoola * manustatakse ka ajumembraanide alla (endolyumbaalselt) meningiidi korral ja kehaõõnde - pleura, kõhu, liigese (koos pleuraga)
artriit, peritoniit ja artriit). Subkutaanselt kasutatavad ravimid infiltraatide purustamiseks. Bensüülpenitsilliini kaaliumisoola * ei saa manustada endovolumbaalselt ega intravenoosselt, kuna ravimist vabanevad kaaliumiioonid võivad põhjustada krampe ja südametegevuse depressiooni.
Pikatoimeliste bensüülpenitsilliini preparaatide (depopenitsilliinide) loomise põhjuseks oli vajadus sagedaste bensüülpenitsilliini naatrium- ja kaaliumsoolade süstimise järele. Vees halva lahustuvuse tõttu moodustavad need ravimid veega suspensioone, neid manustatakse ainult intramuskulaarselt. Depoopenitsilliinid imenduvad süstekohast aeglaselt ega tekita vereplasmas kõrgeid kontsentratsioone, seetõttu kasutatakse neid kerge kuni mõõduka raskusega krooniliste infektsioonide korral.
Pika toimeajaga penitsilliinide hulka kuuluvad bens- ja l-penitsilliin – prokaiintsilliin või bensüülpenitsilliin novokaiini sool*, mis kestab 12-18 tundi, bensatiinbensüülpenitsilliin (bitsilliin-1*), mis kestab 7-10 päeva, ja bitsilliin-5*, millel on antimikroobne toime ühe kuu jooksul.
Fenoksümetüülpenitsilliin erineb keemiliselt bensüülpenitsilliinist selle poolest, et molekulis on bensüülrühma asemel fenoksümetüülrühm, mis muudab selle stabiilseks mao happelises keskkonnas ja sobib suukaudseks manustamiseks.
Looduslikel penitsilliinidel on mõned puudused. Peamised neist on hävitamine penitsillinaasi toimel, ebastabiilsus mao happelises keskkonnas (välja arvatud fenoksümetüülpenitsilliin) ja suhteliselt kitsas toimespekter.
Poolsünteetilised penitsilliinid
6-aminopenitsillaanhappel põhinevate penitsilliinirühma täiustatud antibiootikumide otsimise käigus saadi poolsünteetilisi ravimeid. 6-amino- keemilised modifikatsioonid
penitsillaanhape viidi läbi erinevate radikaalide lisamisega aminorühma. Poolsünteetilised penitsilliinid erinevad looduslikest happekindluse, penitsillinaasi resistentsuse ja toimespektri poolest.
Seal on järgmised poolsünteetiliste penitsilliinide preparaadid.
• Penitsillinaasi suhtes resistentsed kitsa toimespektriga ravimid.
- isoksasolüülpenitsilliinid. Oksatsilliin, dikloksatsilliin.
• Laia toimespektriga ravimid, mis ei ole penitsillinaasi suhtes resistentsed.
- Aminopenitsilliinid. Ampitsilliin, amoksitsilliin.
- Karboksüpenitsilliinid. Karbenitsilliin, karfetsilliin, tikartsilliin.
- Ureidopenitsilliinid.
Aslotsilliin, piperatsilliin, metsotsilliin.
Penitsillinaasi suhtes resistentsed poolsünteetilised penitsilliinid erinevad bensüülpenitsilliini ravimitest selle poolest, et need on efektiivsed penitsillinaasi moodustavate stafülokokkide põhjustatud infektsioonide korral, seetõttu nimetatakse selle rühma ravimeid "stafülokokivastasteks penitsilliinideks". Vastasel juhul vastab toimespekter looduslike penitsilliinide spekterile, kuid aktiivsus on palju madalam.
Oksatsilliin on mao happelises keskkonnas stabiilne, kuid ainult 20-30% ravimist imendub seedetraktist. Märkimisväärne osa seondub verevalkudega. Läbi BBB ei tungi. Ravimit kasutatakse suukaudselt, intramuskulaarselt ja intravenoosselt.
Dikloksatsilliin erineb oksatsilliinist seedetraktist suure imendumise poolest (40-45%).
Aminopenitsilliinid erinevad bensüülpenitsilliini preparaatidest laiema toimespektriga, samuti happeresistentsuse poolest.
Aminopenitsilliinide toimespekter hõlmab nii grampositiivseid kui gramnegatiivseid mikroorganisme (Salmonella, Shigella, Escherichia coli, mõned Proteuse tüved, Haemophilus influenzae). Selle rühma preparaadid ei toimi Pseudomonas aeruginosa ja penitsillinaasi moodustavate stafülokokkide suhtes.
Aminopeitsilliinid kasutatakse ülemiste hingamisteede ägedate bakteriaalsete infektsioonide, bakteriaalse meningiidi, sooleinfektsioonide, sapi- ja kuseteede infektsioonide korral, samuti likvideerimiseks. Helicobacter pylori juures peptiline haavand kõht.
Seedetraktist ampitsilliin imendub mittetäielikult (30-40%). Plasmas seondub vähesel määral (kuni 15-20%) valkudega. Tungib halvasti läbi BBB. See eritub organismist uriini ja sapiga, kus tekib ravimi kõrge kontsentratsioon. Ravimit manustatakse suu kaudu ja intravenoosselt.
Amoksitsilliin on ampitsilliini derivaat, mille farmakokineetika suukaudsel manustamisel on oluliselt paranenud. See imendub seedetraktist hästi (biosaadavus 90-95%) ja suurendab plasmakontsentratsiooni. Kandke ainult sees.
Meditsiinipraktikas kasutatakse kombineeritud preparaate, mis sisaldavad erinevaid ampitsilliini ja oksatsilliini sooli. Nende ravimite hulka kuuluvad Ampiox * (ampitsilliini trihüdraadi ja oksatsilliini naatriumsoola segu vahekorras 1: 1) ja Ampiox-naatrium * (segu naatriumisoolad ampitsilliini ja oksatsilliini vahekorras 2:1). Need ravimid ühendavad laia toimespektri ja resistentsuse penitsillinaasi suhtes. Sellega seoses kasutatakse ampioks * ja ampioks-naatrium * raskete nakkuslikud protsessid(sepsis, endokardiit, sünnitusjärgne infektsioon jne); tuvastamata antibiogrammi ja tuvastamata patogeeniga; grampositiivsete ja gramnegatiivsete mikroorganismide põhjustatud segainfektsiooniga. Ampiox * kasutatakse suukaudselt ja Ampiox-naatrium * manustatakse intramuskulaarselt ja intravenoosselt.
Karboksü- ja ureidopenitsilliinide peamine eelis on aktiivsus Pseudomonas aeruginosa vastu. (Pseudomonas aeruginosa), millega seoses nimetatakse neid penitsilliine "antipseudomonaalseteks". Selle ravimirühma peamised näidustused on Pseudomonas aeruginosa, Proteus, Escherichia coli põhjustatud infektsioonid (sepsis, haavainfektsioonid, kopsupõletik jne).
Karbenitsilliin hävitatakse seedetraktis, mistõttu seda manustatakse intramuskulaarselt ja intravenoosselt. Läbi BBB ei tungi. Umbes 50% ravimist seondub plasmavalkudega. See eritub peamiselt neerude kaudu.
Karfetsilliin, erinevalt karbenitsilliinist, on happekindel ja seda võetakse suu kaudu. Tikartsilliin on aktiivsem kui karbenitsilliin, eriti selle mõju poolest Pseudomonas aeruginosale.
Pseudomonas aeruginosa vastase toime poolest on ureidopenitsilliinid 4–8 korda paremad kui karboksüpenitsilliinid. Neid manustatakse parenteraalselt.
Kõik poolsünteetilised laia toimespektriga penitsilliinid hävitatakse bakteriaalsete β-laktamaaside (penitsillinaaside) toimel, mis vähendab oluliselt nende kliinilist efektiivsust. Selle põhjal saadi ühendid, mis inaktiveerivad bakteriaalseid β-laktamaase. Nende hulka kuuluvad klavulaanhape, sulbaktaam ja tasobaktaam. Need on osa kombineeritud preparaatidest, mis sisaldavad poolsünteetilist penitsilliini ja ühte β-laktamaasi inhibiitoritest. Selliseid ravimeid nimetatakse inhibiitoritega kaitstud penitsilliinideks. Erinevalt monopreparaatidest toimivad inhibiitoriga kaitstud penitsilliinid penitsillinaasi moodustavatele stafülokokkide tüvedele, neil on kõrge aktiivsus β-laktamaasi tootvate gramnegatiivsete bakterite vastu ja need on tõhusad ka bakteroidide vastu.
Farmaatsiatööstus toodab järgmisi kombineeritud preparaate: amoksitsilliin + klavulaanhape (amoksiklav *, augmentiin *), ampitsilliin + sulbaktaam (unasiin *), piperatsilliin + tasobaktaam (tasotsiin *).
Penitsilliini rühma preparaatidel on madal toksilisus ja neil on lai valik ravitoimeid. Küll aga põhjustavad need suhteliselt sageli allergilisi reaktsioone, mis võivad avalduda urtikaaria, nahalööbe, Quincke turse, bronhospasmi ja anafülaktilise šokina. Allergilised reaktsioonid võivad tekkida mis tahes ravimi manustamisviisiga, kuid enamasti arenevad nad koos
parenteraalne manustamine. Allergiliste reaktsioonide ravi seisneb penitsilliini preparaatide kaotamises, samuti sissejuhatuses antihistamiinikumid ja glükokortikoidid. Anafülaktilise šoki korral manustatakse intravenoosselt epinefriini ja glükokortikoide.
Lisaks põhjustavad penitsilliinid mõningaid mitteallergilise iseloomuga kõrvaltoimeid. Neil on ärritav toime. Suukaudsel manustamisel võivad need põhjustada iiveldust, keele- ja suu limaskesta põletikku. Intramuskulaarse süstimise korral võib ilmneda valu ja infiltraadid ning intravenoosse manustamise korral flebiit ja tromboflebiit.
Tsefalosporiinid
Tsefalosporiinid on rühm looduslikke ja poolsünteetilisi antibiootikume, mis põhinevad 7-aminotsefalosporaanhappel.
Vastavalt keemilisele struktuurile on nende antibiootikumide alus (7-aminotsefalosporaanhape) sarnane 6-aminopenitsillaanhappega. Siiski on olulisi erinevusi: penitsilliinide struktuur sisaldab tiasolidiintsüklit ja tsefalosporiinid dihüdrotiasiini ringi.
Tsefalosporiinide ja penitsilliinide struktuursed sarnasused määravad sama antibakteriaalse toime mehhanismi ja tüübi, kõrge aktiivsuse ja efektiivsuse, madala toksilisuse makroorganismile, samuti ristallergilised reaktsioonid penitsilliinidega. Tsefalosporiinide olulised eristavad tunnused on nende resistentsus penitsillinaasi suhtes ja laiaulatuslik antimikroobne toime.
Tsefalosporiine klassifitseeritakse tavaliselt põlvkondade kaupa, mille sees eraldatakse preparaadid parenteraalseks ja enteraalseks manustamiseks (tabel 37-2).
1. põlvkonna tsefalosporiinid
I põlvkonna tsefalosporiinidel on lai toimespekter, millel on valdav toime grampositiivsele taimestikule ning need on spektri ja toime poolest võrreldavad aminopenitsilliinidega. Selle põlvkonna ravimite peamine omadus on nende kõrge stafülokokivastane toime, sealhulgas β-laktamaasi moodustavate tüvede vastu. I põlvkonna tsefalosporiinid mõjutavad mõningaid gramnegatiivseid baktereid (E. coli ja Kleb-
siella), kuid neid hävitavad gramnegatiivsete mikroorganismide β-laktamaasid. Pseudomonas aeruginosa, Proteus, enterokokid ja bakteroidid on peamiselt resistentsed esimese põlvkonna ravimite suhtes.
Tabel 37-2
Tsefalosporiinide klassifikatsioon
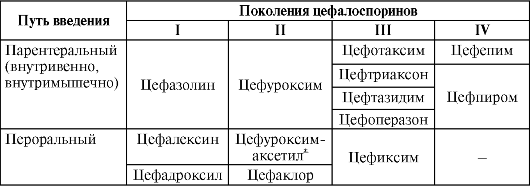
I põlvkonna tsefalosporiine kasutatakse tonsillofarüngiidi, naha ja pehmete kudede infektsioonide, samuti operatsioonijärgsete tüsistuste ennetamiseks.
Tsefasoliin (kefsool *) tungib parenteraalselt manustatuna hästi erinevatesse organitesse ja kudedesse, kuid halvasti läbi BBB. Loob kõrge kontsentratsiooni vereplasmas. See eritub neerude kaudu muutumatul kujul.
Tsefaleksiin (keflex*) on oma toimespektrilt lähedane tsefasoliinile, kuid mõjub halvemini gramnegatiivsetele bakteritele. See imendub seedetraktist hästi, kuid ei tekita kõrgeid kontsentratsioone veres ega enamikus elundites ja kudedes. Terapeutiline kontsentratsioon veres püsib pärast ühekordset süstimist 4-6 tundi.
II põlvkonna tsefalosporiinid
II põlvkonna tsefalosporiinid erinevad I põlvkonna ravimitest suurema aktiivsuse poolest gramnegatiivsete mikroorganismide vastu (E. coli, Proteus, Salmonella, Shigella). Selle põlvkonna preparaadid on gramnegatiivsete bakterite β-laktamaaside toime suhtes vastupidavamad. Nagu esimese põlvkonna tsefalosporiinid, ei mõjuta nad Pseudomonas aeruginosa.
II põlvkonna tsefalosporiine kasutatakse ülemiste ja alumiste hingamisteede bakteriaalsete infektsioonide, kuseteede infektsioonide korral.
radade, naha, pehmete kudede, luude ja liigeste infektsioonide raviks, samuti operatsioonijärgseks antibiootikumide profülaktikaks kirurgias.
Tsefuroksiim (ketocef*) tungib parenteraalselt manustatuna hästi paljudesse organitesse ja kudedesse, sealhulgas läbi BBB (põletiku korral). See eritub peamiselt neerude kaudu.
Tsefuroksiim-aksetiil (tsinnaat*) on eelravimi tsefuroksiimi suukaudne derivaat.
Tsefakloor imendub seedetraktist hästi, tungib paljudesse organitesse ja kudedesse, ei läbi BBB-d. Eritub uriiniga.
3. põlvkonna tsefalosporiinid
III põlvkonna tsefalosporiinid on väga aktiivsed enamiku gramnegatiivsete bakterite, sealhulgas teiste antibiootikumide suhtes resistentsete bakterite vastu. Mõned kolmanda põlvkonna tsefalosporiinid (tseftasidiim, tsefoperasoon) mõjutavad Pseudomonas aeruginosa. Kuid oma toime poolest stafülokokkidele, streptokokkidele ja teistele grampositiivsetele bakteritele jäävad kolmanda põlvkonna tsefalosporiinid alla I-II põlvkonna ravimitele. Kõik selle põlvkonna tsefalosporiinid on resistentsed gramnegatiivsete mikroorganismide β-laktamaaside toime suhtes.
III põlvkonna tsefalosporiinide määramise näidustused hõlmavad erineva lokaliseerimisega infektsioone: ülemised ja alumised hingamisteed, kuseteede, naha, pehmete kudede, sooleinfektsioonid, sepsis, gonorröa, meningiit.
C e f o t a k c ja m (klaforan *) on parenteraalseks manustamiseks mõeldud III põlvkonna tsefalosporiinide peamine esindaja. Ravim tungib hästi erinevatesse kudedesse ja läbib BBB-d. Metaboliseerub maksas. Eritub neerude kaudu. t 1/2 - umbes üks tund.
Tseftriaksoon (longatsef *) on toimespektrilt sarnane tsefotaksiimiga, kuid sellel on pikem t 1/2 (5-7 tundi). Valitud ravim gonorröa ravis.
Tseftasidiim (fortum *) ja tsefoperasoon (tsefobiid *) on Pseudomonas aeruginosa vastu väga aktiivsed, seetõttu kasutatakse neid peamiselt selle patogeeni põhjustatud infektsioonide korral.
IV põlvkonna tsefalosporiinid
IV põlvkonna tsefalosporiinidel on veelgi laiem antimikroobse toime spekter kui III põlvkonna ravimitel. Neid on rohkem
efektiivne grampositiivsete kokkide vastu. Neid iseloomustab suurem vastupidavus β-laktamaaside toimele.
IV põlvkonna tsefalosporiine kasutatakse multiresistentse mikrofloora põhjustatud raskete infektsioonide korral, samuti immuunpuudulikkusega patsientide infektsioonide raviks.
Tsefepiim (maxipiim*) ja tsefperom (Katen*) tungivad parenteraalselt manustatuna hästi paljudesse organitesse ja kudedesse ning läbivad BBB-d. Need erituvad peamiselt muutumatul kujul neerude kaudu.
Tsefalosporiinide kasutamisel on võimalikud allergilised reaktsioonid (urtikaaria, palavik, seerumtõbi, anafülaktiline šokk). Patsientidele, kellel on anamneesis allergilisi reaktsioone penitsilliinide suhtes, ei tohi manustada tsefalosporiine. Mitteallergilistest tüsistustest on võimalik neerufunktsiooni häire, mis on kõige tüüpilisem esimese põlvkonna tsefalosporiinidele. Harvadel juhtudel põhjustavad tsefalosporiinid leukopeeniat. Mõnele tsefalosporiinile, mille struktuuris on 4-metüültiotetrasooli ring (tsefoperasoon jne), on iseloomulik teturamilaadne toime. Suukaudsete tsefalosporiinide võtmisel võivad tekkida düspeptilised sümptomid. Tsefalosporiinide intramuskulaarsel manustamisel võivad ilmneda infiltraadid ja intravenoossel manustamisel - flebiit. Tsefalosporiinide võtmisel tuleb arvestada superinfektsiooni tekke võimalusega.
Karbapeneemid
Karbapeneemid kuuluvad β-laktaamantibiootikumide rühma. Neid iseloomustab suurem resistentsus β-laktamaaside toime suhtes ja neil on lai antibakteriaalse toime spekter, sealhulgas III ja IV põlvkonna tsefalosporiinide suhtes resistentsed tüved.
Karbapeneemid on reservantibiootikumid, neid kasutatakse multiresistentsete mikroorganismitüvede põhjustatud raskete infektsioonide korral.
Karbapeneemide hulka kuuluvad imipeneem ja meropeneem.
I mipeneem on tienamütsiini derivaat, mida toodab Streptomyces cattleya. Sest meditsiiniliseks kasutamiseks toota kombineeritud ravimit, mis sisaldab imipeneemi koos neerutuubulite dehüdropeptidaas I spetsiifilise inhibiitoriga - tsilastatiiniga. See kombinatsioon inhibeerib imipeneemi metabolismi neerudes ja suurendab oluliselt muutumatul kujul imipeneemi kontsentratsiooni
antibiootikumid neerudes ja kuseteedes. Seda kombineeritud ravimit nimetatakse tienaamiks*.
Tien a m * manustatakse intravenoosselt. See tungib hästi paljudesse organitesse ja kudedesse, läbib BBB-d ajukelme põletiku ajal.
on 1 tund.Ravimi kasutamisel on võimalikud allergilised reaktsioonid, iiveldus, oksendamine, krambid.
Meropeneem (Meronem *), erinevalt imipeneemist, ei hävita neerutuubulite dehüdropeptidaas, seetõttu kasutatakse seda ilma selle inhibiitoriteta. Teiste omaduste poolest on see lähedane imipeneemile.
Monobaktaamid
Selle rühma antibiootikumide struktuuris on monotsükliline β-laktaamtsükkel. Monobaktaamidest on meditsiinipraktikas kasutusel üks antibiootikum, astreonaam. Ravim on väga aktiivne gramnegatiivsete bakterite (Escherichia ja Pseudomonas aeruginosa, Proteus, Klebsiella jt) vastu ning ei mõjuta grampositiivseid baktereid, bakteroide ja muid anaeroobe.
Astreonaami antimikroobse toimespektri eripära on tingitud asjaolust, et see on resistentne paljude gramnegatiivse taimestiku poolt toodetud β-laktamaaside suhtes ja samal ajal hävitatakse grampositiivsete mikroorganismide ja bakterioidide β-laktamaaside poolt.
Aztreonaam on reservravim, seda kasutatakse raskete kuseteede infektsioonide korral, kõhuõõnde ja väike vaagen, meningiit, sepsis, koos teiste antibakteriaalsete ainete ebaefektiivsusega. Ravimit manustatakse intramuskulaarselt või intravenoosselt. Kõrvaltoimetest täheldati düspeptilisi häireid, naha allergilisi reaktsioone, peavalu.
Makroliidid ja nendega seotud antibiootikumid
Makroliidid on antibiootikumide klass, mille keemiline struktuur põhineb makrotsüklilisel laktoonitsüklil, mis on seotud erinevate suhkrutega.
Makroliidid klassifitseeritakse sõltuvalt valmistamismeetoditest ja süsinikuaatomite arvust makrotsüklilises laktoonitsüklis (tabel 37-3).
Tabel 37-3
Makroliidide klassifikatsioon

Makroliide iseloomustavad järgmised üldised omadused.
• Võimalus häirida mikroobsete valkude sünteesi ribosoomide tasemel. Nad seostuvad bakteriaalsete ribosoomide 50S alaühikuga ja häirivad peptiidsidemete moodustumist (inhibeerivad translokatsiooni protsessi). Mikroorganismide resistentsus makroliidide suhtes on seotud muutustega bakteriaalsete ribosoomide 50S alaühikute retseptorite struktuuris, mis häirib antibiootikumi seondumist ribosoomidega.
• Valdavalt bakteriostaatiline toime. Suures kontsentratsioonis on neil bakteritsiidne toime pneumokokkide, läkaköha ja difteeria patogeenidele.
• Kõrge aktiivsus grampositiivsete kokkide (streptokokid, stafülokokid) ja rakusiseste patogeenide (klamüüdia ja mükoplasmad) vastu.
• Võime tungida rakkudesse ja tekitada kõrgeid intratsellulaarseid kontsentratsioone.
• Madal toksilisus makroorganismidele.
• β-laktaamantibiootikumidega ristallergilisi reaktsioone ei esine.
Makroliidide toimespekter hõlmab:
• grampositiivsed kokid (streptokokid, stafülokokid);
• grampositiivsed vardad (difteeria, listeria tekitajad);
• gramnegatiivsed kookid (gonokokid, meningokokid);
• gramnegatiivsed vardad (legionella, helikobakterid);
• klamüüdia, mükoplasma, spiroheedid.
Seega meenutavad makroliidid antimikroobse toime spektri poolest bensüülpenitsilliini preparaate.
Makroliide kasutatakse streptokoki tonsillofarüngiidi, kopsupõletiku (sealhulgas mükoplasmade, klamüüdia ja legionella põhjustatud ebatüüpilise kopsupõletiku), läkaköha, difteeria, sarlakid, naha ja pehmete kudede infektsioonide, klamüüdia, mükoplasma infektsiooni, suuõõne infektsioonide ja ka reuma (penitsilliinide allergiaga) aastaringseks ennetamiseks.
Erütromütsiin on looduslik makroliid, mida toodab Streptomyces erythreus. Suukaudsel manustamisel imendub ravim seedetraktist aeglaselt, hävides osaliselt mao happelises keskkonnas.
Toidu juuresolekul väheneb biosaadavus järsult. Hästi satub bronhide saladusse, sapi. Läbib halvasti BBB-d. See eritub peamiselt seedetrakti kaudu. Toime kestus on 4-6 tundi.
Oleandomütsiini sünteesiprodukt Streptomyces antibiootikum. Toimespekter on sarnane erütromütsiiniga, kuid vähem aktiivne.
Roksitromütsiin (ruliid*) ja klaritromütsiin (klatsiid*) on poolsünteetilised 14-meerilised makroliidid. Erinevalt erütromütsiinist imenduvad need seedetraktist hästi, samas kui toit ei mõjuta ravimite imendumist. Looge kudedes kõrge kontsentratsioon. Need kestavad kauem. t 1/2 roksitromütsiin on 13 tundi, klaritromütsiin - 3-4 tundi.Rakendatakse sees.
Lisaks ülaltoodud näidustustele kasutatakse likvideerimiseks klaritromütsiini Helicobacter pylori maohaavandiga ja kaksteistsõrmiksool, samuti AIDSi atüüpilise mükobakterioosi ennetamiseks ja raviks.
Asitromütsiin (sumamed *) on poolsünteetiline 15-liikmeline makroliid, mis kuulub asaliidide alamklassi, kuna makrotsüklilises
milline tsükkel sisaldab lämmastikuaatomit. Erinevalt erütromütsiinist on see gramnegatiivsete mikroorganismide vastu aktiivsem. Loob makroliidide seas kõrgeima kontsentratsiooni kudedes. Ravimil on pikk t 1/2 - kuni 35-55 tundi, mis võimaldab ravimit välja kirjutada üks kord päevas.
Spiramütsiin, josamütsiin ja midekamütsiin on looduslikud 16-meerilised makroliidid. Ravimid on tõhusad mõnede erütromütsiini suhtes resistentsete streptokokkide ja stafülokokkide tüvede vastu. Need imenduvad seedetraktist hästi, samas kui toit praktiliselt ei mõjuta biosaadavust. Midekamütsiinatsetaat on poolsünteetiline antibiootikum, millel on täiustatud farmakokineetika.
Selle rühma ravimite kõrvaltoimed on peamiselt allergilised reaktsioonid ja düspeptilised häired.
Linkosamiidid
Linkosamiidide rühma kuuluvad looduslik antibiootikum linkomütsiin ja selle poolsünteetiline analoog klindamütsiin.
Linkosamiididel on järgmised üldised omadused:
• võime inhibeerida valkude sünteesi mikroobirakus (toimivad nagu makroliidid);
• valdavalt bakteriostaatiline toime. Kõrgetes kontsentratsioonides võivad need grampositiivsetele kokkidele bakteritsiidselt mõjuda;
• kitsas toimespekter (peamiselt grampositiivsed kokid, sealhulgas penitsillinaasi moodustavad stafülokokkide tüved). Väga aktiivne bakteroidide vastu – kohustuslikud eoseid mittemoodustavad anaeroobid;
• võime akumuleeruda luukoe ja liigesed;
• mikrofloora resistentsuse kiire areng;
• β-laktaamantibiootikumidega ei esine ristallergilisi reaktsioone.
Linkosamiide kasutatakse antistafülokokkide reservravimitena tonsillofarüngiidi, kopsupõletiku, naha-, pehmete kudede, luude ja liigeste infektsioonide, aga ka bakteroidide põhjustatud infektsioonide korral.
Linkomütsiin imendub seedetraktist, samal ajal kui toit häirib ravimi imendumist. Metaboliseerub maksas, eritub peamiselt sapiga.
Klindamütsiin (dalacin C*) on aktiivsem kui linkomütsiin. Suurtes annustes toimib see Toxoplasmale ja Plasmodiumile, seega täiendavad näidustused kasutamiseks - troopiline malaaria (kombinatsioonis kiniiniga) ja toksoplasmoos (koos pürimetamiiniga). Klindamütsiini biosaadavus on kõrgem, sõltumata toidu tarbimisest.
Linkosamiidide kasutamisel võivad tekkida düspeptilised häired ja allergilised reaktsioonid.
Kõige raskem kõrvaltoime on pseudomembranoosne koliit, mis areneb spoore mittemoodustatava anaeroobse soolefloora ja paljunemise pärssimise tulemusena. Clostridium difficile, toodavad enterotoksiine, mis põhjustavad soole seinas hävitavaid muutusi. Koliit on raske kulgemisega, iseloomulikud on haavandid kuni sooleperforatsiooni ja peritoniidi tekkeni. Koliidi raviks määratakse suukaudselt vankomütsiin või metronidasool, samuti viiakse läbi võõrutusravi.
Aminoglükosiidid
Aminoglükosiidi molekul põhineb tsüklilisel alkoholil - aminotsüklitoolil, millele on kinnitatud aminosuhkrud. Aminoglükosiidide rühma esindavad looduslikud ja poolsünteetilised ravimid, mis liigitatakse tavaliselt põlvkondade kaupa.
• I põlvkonna aminoglükosiidid.
Streptomütsiin, neomütsiin, kanamütsiin.
• II põlvkonna aminoglükosiidid.
Gentamütsiin, tobramütsiin, sisomütsiin.
• III põlvkonna aminoglükosiidid.
Amikatsiin.
Kõik aminoglükosiidid on oma omadustelt sarnased ja erinevad peamiselt aktiivsuse, toimespektri, kõrvaltoimete tõsiduse ja mikroorganismide resistentsuse poolest.
Aminoglükosiidide üldised omadused on järgmised:
• võime häirida valkude sünteesi mikroobirakus. Aminoglükosiidid seonduvad bakteriraku ribosoomi 30S subühikuga, mis häirib ribosoomi liikumist mööda messenger-RNA ahelat. Aminoglükosiidid häirivad ka mRNA koodi lugemise protsesse, mis viib funktsionaalselt inaktiivsete valkude sünteesini;
• võime häirida mikroorganismide tsütoplasmaatilise membraani läbilaskvust;
• bakteritsiidne toime;
• penitsilliinide ja tsefalosporiinide antibakteriaalse toime tugevdamine;
• lai valik antibakteriaalset toimet, millel on domineeriv toime gramnegatiivsele taimestikule;
• kõrge toksilisus inimesele, mis väljendub spetsiifilises kahjustuses neerudele (nefrotoksiline toime), kuulmis- ja vestibulaaraparaadile (ototoksiline toime), neuromuskulaarse ülekande pärssimises, mis väljendub nõrgenenud hingamises, lihastoonuse languses ja motoorne funktsioon;
• sarnased farmakokineetilised omadused - aminoglükosiidid praktiliselt ei imendu seedetraktist (väga hüdrofiilsed), läbivad halvasti histohemaatilisi barjääre, praktiliselt ei metaboliseeru ja erituvad neerude kaudu muutumatul kujul, luues kõrge kontsentratsiooni uriinis.
Aminoglükosiidide toimespekter hõlmab paljusid grampositiivseid ja gramnegatiivseid mikroorganisme (stafülokokid, streptokokid, pneumokokid, E. coli, salmonella, shigella, klebsiella, proteus, enterobakterid, Pseudomonas aeruginosa). Esimese põlvkonna aminoglükosiidid avaldavad pärssivat mõju mycobacterium tuberculosis, tulareemia ja katku tekitajad. Anaeroobid, spiroheedid ja algloomad ei ole aminoglükosiidide suhtes tundlikud.
Aminoglükosiide kasutatakse gramnegatiivsete mikroorganismide, Pseudomonas aeruginosa, aga ka tuberkuloosi, katku, tulareemia, brutselloosi põhjustatud erineva lokaliseerimisega infektsioonide korral.
Esimese põlvkonna aminoglükosiide kasutatakse praegu mikrofloora resistentsuse kiire arengu ja kõrge toksilisuse tõttu piiratud ulatuses.
Streptomütsiini kasutatakse tuberkuloosi ja eriti ohtlike infektsioonide (katk, tulareemia) raviks kombinatsioonis tetratsükliiniga. Ravimit manustatakse kõige sagedamini intramuskulaarselt. Streptomütsiinil on väljendunud ototoksiline toime.
Neomütsiin on kõige ototoksilisem aminoglükosiid. Seda kasutatakse suu kaudu soolte puhastamiseks operatsioonideks valmistumisel
Seedetrakt (neomütsiin ei imendu soolestikus) ja paikselt mädaste nahakahjustuste (püoderma, nakatunud ekseem jne) raviks. Väliselt kasutatakse neomütsiini mõnikord koos glükokortikoididega (sisaldub kombineeritud salvides locacorten-N *, sinalar H * jne). Parenteraalseks manustamiseks ei kasutata ravimit kõrge toksilisuse tõttu.
Kanamütsiini kasutatakse suukaudselt samadel näidustustel nagu neomütsiini ja parenteraalselt tuberkuloosi raviks.
Teise põlvkonna aminoglükosiidid on väga aktiivsed Pseudomonas aeruginosa ja mõnede teiste mikroorganismide vastu, mis on resistentsed esimese põlvkonna ravimite ja teiste rühmade antibiootikumide suhtes. Selle põlvkonna ravimite suhtes areneb resistentsus aeglasemalt.
Teise põlvkonna aminoglükosiidide peamine esindaja on geen t ja mütsiin. Ravimit kasutatakse peamiselt raskete infektsioonide (sepsis, kopsupõletik, endokardiit, kuseteede infektsioonid jne) korral, mida põhjustavad gramnegatiivsed bakterid, mis on resistentsed teistele antibiootikumidele. Ravimit manustatakse intramuskulaarselt ja intravenoosselt. Gentamütsiini kasutatakse ka paikselt nakatunud haavade ja põletuste raviks. Gentamütsiini kasutamisel tekivad aminoglükosiididele omased kõrvaltoimed.
Tobramütsiin ja sisomütsiin on oma omadustelt sarnased gentamütsiiniga.
Amikatsiin on kolmanda põlvkonna aminoglükosiid. Erinevalt gentamütsiinist toimib amikatsiin paljudele gramnegatiivsete bakterite tüvedele, mis on resistentsed teise põlvkonna aminoglükosiidide suhtes, kuna seda ei inaktiveerita bakteriaalsete ensüümide poolt. Ravimit kasutatakse kõige raskemate infektsioonide raviks, mis on põhjustatud mitmekordsest resistentsest mikrofloorast. Sisestage intramuskulaarselt ja intravenoosselt.
Aminoglükosiidide parenteraalsel kasutamisel on vajalik neerufunktsiooni, kuulmise ja vestibulaarsüsteemi süstemaatiline jälgimine. Aminoglükosiidid on vastunäidustatud neerude ja kuulmisnärvi haiguste, raseduse, myasthenia gravis'e korral.
Tetratsükliinid
Tetratsükliinide rühma kuuluvad looduslikud ja poolsünteetilised antibiootikumid, mille struktuurne alus on neli kokkusulanud kuueliikmelist tsüklit.
Klassifitseerige tetratsükliinid sõltuvalt valmistamismeetodist.
• Looduslikud (biosünteetilised) antibiootikumid.
Tetratsükliin, oksütetratsükliin.
• Poolsünteetilised antibiootikumid.
Metatsükliin (rondamütsiin*), doksütsükliin (vibramütsiin*). Üldised omadused tetratsükliinid on:
• võime pärssida mikroobsete valkude sünteesi ribosoomide tasemel. Tetratsükliinid seonduvad bakteriaalsete ribosoomide 30S subühikuga, mille tulemusena polüpeptiidahela pikenemise protsess peatatakse;
• bakteriostaatiline toime. Tetratsükliinid on kõige aktiivsemad vohavate mikroorganismide vastu;
• lai valik antimikroobset toimet;
• kõrge aktiivsus rakusiseste mikroorganismide vastu;
• kõrge lipofiilsus, mis tagab ravimite suure imendumise seedetraktist, võime ületada bioloogilisi barjääre ja akumuleeruda kudedesse;
• võime siduda kelaatkompleksideks kahevalentsed ioonid - raud, kaltsium, magneesium, tsink.
Laia toimespektriga antibiootikumidena kasutatakse tetratsükliine paljude nakkushaiguste korral. Esiteks on tetratsükliinid näidustatud brutselloosi, riketsioosi (tüüfus, Q-palavik jne), katku, koolera, tulareemia korral. Tetratsükliine on ette nähtud Escherichia coli (peritoniit, koletsüstiit jne), shigella (batsillaarne düsenteeria), spiroheetide (süüfilis), klamüüdia (trahhoom, ornitoos, urogenitaalne klamüüdia jne), mükoplasmade (SARS-i tekitajad) põhjustatud haiguste korral. Tetratsükliine kasutatakse ka likvideerimiseks Helicobacter pylori mao ja kaksteistsõrmiksoole peptilise haavandiga.
Tetratsükliinide laialdane kasutamine meditsiinipraktikas on toonud kaasa suure hulga nende antibiootikumide suhtes resistentsete stafülokokkide, enterokokkide, stafülokokkide ja pneumokokkide tüvede tekkimise. Samal ajal areneb ristresistentsus kõigi tetratsükliini seeria ravimite suhtes.
Selle rühma ravimite antibakteriaalse toime kestus ei ole sama. Selle põhjal tuleks nende hulgas eristada:
• lühitoimelised tetratsükliinid (6-8 tundi) - tetratsükliin ja oksütetratsükliin;
• pika toimeajaga tetratsükliinid (12-24 tundi) - metatsükliin ja doksütsükliin.
Tetratsükliine manustatakse tavaliselt suukaudselt (kapslites või kaetud tablettidena). Lühitoimelised preparaadid on ette nähtud neli korda päevas, pika toimeajaga - 1-2 korda päevas. Lisaks kl rasked vormid ah mädased-septilised haigused, tetratsükliinide lahustuvad soolad manustatakse parenteraalselt (intramuskulaarselt, intravenoosselt, kehaõõnde).
Tetratsükliinide kasutamisel tekivad sageli allergilise ja mitteallergilise iseloomuga kõrvaltoimed. Allergiliste reaktsioonide kõige levinum ilming on nahalööve ja urtikaaria, harvadel juhtudel võib tekkida angioödeem ja anafülaktiline šokk.
Mitteallergilise iseloomuga kõrvaltoimetest tuleb märkida limaskestade ärritavat toimet. seedetrakt(iiveldus, oksendamine, kõhuvalu, kõhupuhitus, kõhulahtisus) suukaudsel manustamisel ja intravenoossel manustamisel kokkupuutel veeniseinaga tromboflebiidi teke.
Tetratsükliinidel on hepatotoksiline toime, mis on eriti väljendunud maksafunktsiooni rikkumise korral.
Selle rühma antibiootikumidel on üldine kataboolne toime: nad pärsivad valgusünteesi, soodustavad aminohapete, vitamiinide ja muude ühendite väljutamist organismist.
Tetratsükliinid ladestuvad luukoesse, sh hammaste kudedesse ning moodustavad kaltsiumiga vähelahustuvaid komplekse, millega seoses on häiritud luustiku moodustumine, hammaste määrdumine ja kahjustus. Sel põhjusel ei tohi tetratsükliine anda alla 12-aastastele lastele ja rasedatele naistele.
Tetratsükliinide iseloomulik kõrvaltoime on düsbakterioos ja superinfektsioon suuõõne ja muud tüüpi kanalite esinemisel.
didoos. Harva võib tekkida pseudomembranoosne enterokoliit.
Tetratsükliinid on vastunäidustatud raseduse, imetamise, maksa ja neerude raske patoloogia ajal.
37.2. SÜNTEETILISED ANTIBAKTERIAALID
Paljud sünteetilised ained erinevatest keemiliste ühendite klassidest omavad antibakteriaalset toimet. Nende hulgas on suurima praktilise väärtusega järgmised uimastirühmad.
• Sulfoonamiidid.
• kinolooni derivaadid.
• Nitrofuraani derivaadid.
• 8-hüdroksükinoliini derivaadid.
• Kinoksaliini derivaadid.
• Oksasolidinoonid.
Sulfanilamiidi preparaadid
Sulfanilamiidi preparaadid hõlmavad ühendeid, millel on ühine struktuurvalem.
Sulfoonamiide võib pidada sulfaniilhappeamiidi derivaatideks.
Kemoterapeutiline aktiivsus sulfa ravimid avastas esmakordselt 1935. aastal saksa arst ja teadlane G. Domagk, kes avaldas andmed kliinikus värvainena sünteesitud prontosiili (punase streptotsiidi) eduka kasutamise kohta. Peagi tehti kindlaks, et punase streptotsiidi toimeaine on metabolismi käigus moodustunud sulfoonamiid (streptotsiid *).

Seejärel sünteesiti sulfaniilamiidi molekuli põhjal suur hulk selle derivaate, millest osa
kätte saanud lai rakendus meditsiinis. Sulfoonamiidide erinevate modifikatsioonide süntees viidi läbi tõhusamate, pikaajalise toimeajaga ja vähem toksiliste ravimite loomise suunas.
Taga viimased aastad sulfoonamiidide kasutamine kliinilises praktikas on vähenenud, kuna need on aktiivsuselt oluliselt madalamad kui kaasaegsed antibiootikumid ja neil on suhteliselt kõrge toksilisus. Lisaks on sulfoonamiidide pikaajalise, sageli kontrollimatu ja põhjendamatu kasutamise tõttu enamikul mikroorganismidel tekkinud nende suhtes resistentsus.
Sulfoonamiididel on mikroorganismidele bakteriostaatiline toime. Sulfoonamiidide bakteriostaatilise toime mehhanism seisneb selles, et need ained, millel on struktuurne sarnasus para-aminobensoehappega, konkureerivad sellega sünteesi ajal. foolhape- mikroorganismide kasvufaktor.
Sulfoonamiidid inhibeerivad konkureerivalt dihüdropteroaadi süntetaasi ja takistavad ka para-aminobensoehappe liitumist dihüdrofoolhappega. Dihüdrofoolhappe sünteesi rikkumine vähendab sellest tetrahüdrofoolhappe moodustumist, mis on vajalik puriini ja pürimidiini aluste sünteesiks (joonis 37-1). Selle tulemusena pärsitakse nukleiinhapete sünteesi, mis põhjustab mikroorganismide kasvu ja paljunemise pärssimist.
Sulfoonamiidid ei häiri dihüdrofoolhappe sünteesi makroorganismi rakkudes, kuna viimased ei sünteesi, vaid kasutavad valmis dihüdrofoolhapet.
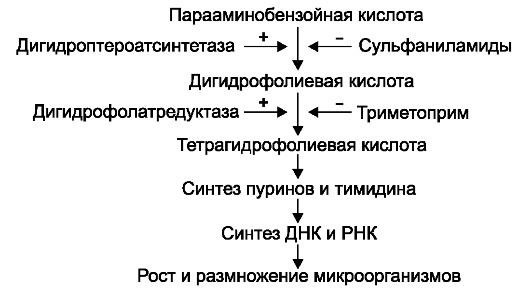
Riis. 37-1. Ko-trimoksasooli toimemehhanism
Keskkondades, kus on palju paraaminobensoehapet (mäda, kudede detritus), on sulfoonamiidid ebaefektiivsed. Samal põhjusel toimivad nad nõrgalt prokaiini (novokaiin*) ja bensokaiini (anestesiin*) juuresolekul, mis hüdrolüüsitakse paraaminobensoehappeks.
Sulfoonamiidide pikaajaline kasutamine põhjustab mikroorganismide resistentsuse tekkimist.
Algselt olid sulfoonamiidid aktiivsed paljude grampositiivsete ja gramnegatiivsete bakterite vastu, kuid nüüdseks on paljud stafülokokkide, streptokokkide, pneumokokkide, gonokokkide, meningokokkide tüved muutunud resistentseks. Sulfoonamiidid säilitasid oma aktiivsuse nokardia, toksoplasma, klamüüdia, malaaria plasmoodia ja aktinomütseedi vastu.
Peamised näidustused sulfoonamiidide määramiseks: nokardioos, toksoplasmoos, klorokviinile resistentne troopiline malaaria. Mõnel juhul kasutatakse sulfoonamiide kookosnakkuste, bakteriaalse düsenteeria, Escherichia coli põhjustatud infektsioonide korral.
Sulfoonamiidid praktiliselt ei erine üksteisest toimespektri poolest. Peamine erinevus sulfoonamiidide vahel seisneb nende farmakokineetilistes omadustes.
• Sulfoonamiidid resorptiivseks toimeks(imendub hästi seedetraktist).
- Lühilavastus (t 1/2< 10 ч).
Sulfanilamiid (streptotsiid*), sulfatiasool (norsulfasool*), sulfatidool (etasool*), sulfakarbamiid (urosulfaan*), sulfadimidiin (sulfadimesiin*).
- keskmise kestusega toimingud (t 1/2 10-24 tundi). Sulfadiasiin (sulfasiin), sulfametoksasool.
- Pikatoimeline (t 1/2 24-48 tundi). Sulfadimetoksiin, sulfamometoksiin.
- Ülipikk tegevus (t 1/2> 48 h). Sulfalen.
• Sulfoonamiidid, mis toimivad soolestiku luumenis (seedetraktist halvasti imenduvad).
Ftalüülsulfatiasool (ftalasool*), sulfaguanidiin (sulgin*).
• Sulfoonamiidid kohalikuks kasutamiseks.
Sulfatseetamiid (sulfatsüülnaatrium*), hõbesulfadiasiin, hõbesulfatiasool (argosulfaan*).
• Sulfoonamiidide ja salitsüülhappe kombineeritud preparaadid.
Sulfasalasiin, mesalasiin (salasopüridasiin*), salasodimetoksiin*.
• Sulfoonamiidide kombineeritud preparaadid trimetoprimiga.
Ko-trimoksasool (baktrim*, biseptool*), lidaprim*, sulfatoon*, poteseptil*.
Resorptiivse toimega ravimid imenduvad seedetraktist hästi. Suurima kontsentratsiooni veres loovad lühikese ja keskmise toimeajaga preparaadid. Pika- ja ülipika toimeajaga ravimid seonduvad suuremal määral vereplasma valkudega. Sulfoonamiidid jaotuvad kõigis kudedes, läbivad BBB-d, platsentat ja kogunevad keha seroossetesse õõnsustesse. Peamine sulfoonamiidide muundamise tee organismis on atsetüülimine, mis toimub maksas. Atsetüülimise aste jaoks erinevad ravimid ei ole sama. Atsetüülitud metaboliidid on farmakoloogiliselt inaktiivsed. Atsetüülitud metaboliitide lahustuvus on oluliselt halvem kui algsetel sulfoonamiididel, eriti uriini happeliste pH väärtuste korral, mis võib põhjustada kristallide (kristalluuria) moodustumist uriinis. Sulfoonamiidid ja nende metaboliidid erituvad peamiselt neerude kaudu.
S u l f a n i l a m i d on üks esimesi sulfaniilamiidstruktuuriga antimikroobseid preparaate. Praegu ravimit praktiliselt ei kasutata selle madala efektiivsuse ja kõrge toksilisuse tõttu.
Sulfatiasooli, sulfatidooli, sulfadimidiini ja sulfakarbamiidi kasutatakse 4-6 korda päevas. Urosulfaani* kasutatakse kuseteede infektsioonide raviks, kuna ravim eritub muutumatul kujul neerude kaudu ja tekitab uriinis kõrge kontsentratsiooni. Sulfametoksasool on osa kombineeritud ravimist kotrimoksasool *. Sulfamonometoksiin ja sulfadimetoksiin määratakse 1-2 korda päevas.
Sulfaleeni kasutatakse iga päev ägedate või kiiresti esinevate nakkusprotsesside korral, üks kord 7-10 päeva jooksul - krooniliste, pikaajaliste infektsioonide korral.
Resorptiivse toimega sulfoonamiidid põhjustavad palju kõrvaltoimeid. Nende kasutamine võib põhjustada veresüsteemi häireid (aneemia, leukopeenia, trombotsütopeenia), hepatotoksilisust, allergilisi reaktsioone (nahalööbed, palavik, agranulaarne
tsütoos), düspeptilised häired. Uriini happelise pH väärtuse korral on kristalluuria võimalik. Kristalluuria tekke vältimiseks tuleb sulfoonamiide võtta koos leelisega mineraalvesi või sooda lahusega.
Sulfoonamiidid, mis toimivad soolestiku luumenis, ei imendu seedetraktis praktiliselt ja tekitavad soolestiku luumenis kõrge kontsentratsiooni, seetõttu kasutatakse neid sooleinfektsioonide (šigelloos, enterokoliit) ravis, aga ka sooleinfektsioonide ennetamiseks. sisse operatsioonijärgne periood. Kuid praegu on paljud sooleinfektsioonide patogeenide tüved muutunud sulfoonamiidide suhtes resistentseks. Ravi efektiivsuse suurendamiseks samaaegselt soolestiku luumenis toimivate sulfoonamiididega on soovitatav välja kirjutada hästi imenduvad ravimid (etasool * , sulfadimesiin * jne), kuna sooleinfektsioonide tekitajad ei paikne mitte ainult luumenis, aga ka sooleseinas. Selle rühma ravimite võtmisel tuleb välja kirjutada B-rühma vitamiinid, kuna sulfoonamiidid pärsivad kasvu coli osaleb selle rühma vitamiinide sünteesis.
Ftalüülsulfatiasoolil on pärast ftaalhappe eliminatsiooni ja aminorühma vabanemist antimikroobne toime. Ftalüülsulfatiasooli toimeaine on norsulfasool*.
Ftalüülsulfatiasool määratakse 4-6 korda päevas. Ravimil on madal toksilisus. Kõrvaltoimeid praktiliselt pole.
Sulfaguanidiin on oma toimelt sarnane ftalüülsulfatiasooliga.
Sulfatsetaam ja d-sulfanilamiid paikseks kasutamiseks, mida kasutatakse oftalmoloogilises praktikas lahuste (10-20-30%) ja salvidena (10-20-30%) konjunktiviidi, blefariidi, sarvkesta mädaste haavandite ja gonorröa korral. silmahaigused. Tavaliselt taluvad patsiendid ravimit hästi. Mõnikord, eriti kontsentreeritumate lahuste kasutamisel, ärritav
tegevus; sellistel juhtudel on ette nähtud madalama kontsentratsiooniga lahused.
Hõbesulfadiasiin ja hõbesulfatiasool eristuvad selle poolest, et molekulis on hõbeda aatom, mis suurendab nende antibakteriaalset toimet. Preparaate kasutatakse paikselt salvide kujul põletushaavade ja haavainfektsioonid, troofilised haavandid, lamatised. Ravimite kasutamisel võivad tekkida allergilised nahareaktsioonid.
To kombineeritud preparaadid, mis ühendab oma struktuuris sulfaniilamiidi ja salitsüülhappe fragmente, sealhulgas sulfasalasiini, salasopüridasiin * , salasodimetoksiin * . Käärsooles hüdrolüüsitakse need ühendid mikrofloora mõjul 5-aminosalitsüülhappeks ja sulfaniilamiidkomponendiks. Kõigil neil ravimitel on antibakteriaalne ja põletikuvastane toime. Neid kasutatakse mittespetsiifilisteks haavandiline jämesoolepõletik ja Crohni tõbi, samuti põhilised vahendid reumatoidartriidi ravis.
Sulfasalasiin on sulfapüridiini asoühend koos salitsüülhape. Ravim on ette nähtud sees. Ravimi võtmisel võivad tekkida allergilised reaktsioonid, düspeptilised sümptomid, põletustunne pärasooles, leukopeenia.
Salasopüridasiin* ja salasodimetoksiin* omavad sarnaseid omadusi.
Trimetoprim on pürimidiini derivaat, millel on bakteriostaatiline toime. Ravim blokeerib dihüdrofolaatreduktaasi inhibeerimise tõttu dihüdrofoolhappe redutseerumist tetrahüdrofoolhappeks.
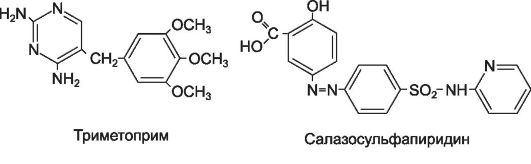
Trimetoprimi afiinsus bakteriaalse dihüdrofolaadi reduktaasi suhtes on 50 000 korda kõrgem kui imetajate dihüdrofolaadi reduktaasi suhtes.
Trimetoprimi kombinatsiooni sulfoonamiididega iseloomustab bakteritsiidne toime ja lai spekter antibakteriaalseid toimeid.
toimed, sealhulgas paljude antibiootikumide ja tavaliste sulfoonamiidide suhtes resistentne mikrofloora.
Enamik kuulus ravim Sellesse rühma kuuluv ko-trimoksasool on kombinatsioon viiest osast sulfametoksasoolist (keskmise toimeajaga sulfoonamiid) ja ühest osast trimetoprimist. Sulfametoksasooli valimine kotrimoksasooli komponendiks on tingitud asjaolust, et sellel on sama eliminatsioonikiirus kui trimetoprimil.
Ko-trimoksasool imendub seedetraktist hästi, tungib paljudesse organitesse ja kudedesse, tekitab kõrge kontsentratsiooni bronhide eritises, sapis, uriinis ja eesnäärmes. Tungib läbi BBB, eriti ajukelme põletiku korral. See eritub peamiselt uriiniga.
Ravimit kasutatakse hingamisteede ja kuseteede infektsioonide, kirurgiliste ja haavainfektsioonide, brutselloosi korral.
Ravimi kasutamisel tekivad resorptiivsetele sulfoonamiididele iseloomulikud kõrvaltoimed. Ko-trimoksasool on vastunäidustatud raskete maksa-, neeru- ja vereloomehäirete korral. Ravimit ei tohi raseduse ajal välja kirjutada.
Sarnased ravimid: lidaprim* (sulfametrool + trimetoprim), sulfatoon* (sulfamonometoksiin + trimetoprim), poteseptil* (sulfadimidiin + trimetoprim).
Kinolooni derivaadid
Kinolooni derivaadid on esindatud fluorimata ja fluoritud ühenditega. Kõige kõrgem antibakteriaalne toime on ühenditel, mis sisaldavad asendamata või asendatud piperasiinitsüklit kinoloonituuma positsioonis 7 ja fluori aatomit positsioonis 6. Neid ühendeid nimetatakse fluorokinoloonideks.
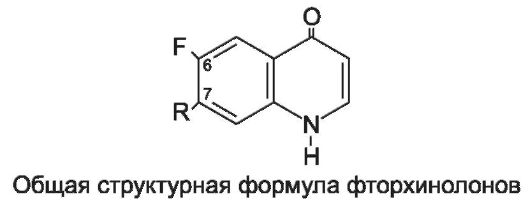
Kinolooni derivaatide klassifikatsioon.
• fluoreerimata kinoloonid.
Nalidiksiinhape (nevigramon*, negram*), oksoliinhape (gramuriin*), pipemiidhape (paliin*).
• Fluorokinoloonid(esimese põlvkonna preparaadid).
Tsiprofloksatsiin (Cifran*, Ciprobay*), lomefloksatsiin (maksakiin*), norfloksatsiin (nolitsiin*), ofloksatsiin (Tarivid*), enoksatsiin (enoksor*), pefloksatsiin (abaktal*).
• Fluorokinoloonid(uued teise põlvkonna ravimid).
Levofloksatsiin (tavanic*), sparfloksatsiin, moksifloksatsiin. Fluorimata kinoloonide rühma esivanem - na l ja -
diksiinhape. Ravim on aktiivne ainult teatud gramnegatiivsete mikroorganismide vastu - Escherichia coli, Shigella, Klebsiella, Salmonella. Pseudomonas aeruginosa on nalidiksiinhappe suhtes resistentne. Mikroorganismide resistentsus ravimi suhtes tekib kiiresti.
Ravim imendub seedetraktis hästi, eriti tühja kõhuga. Ravimi kõrge kontsentratsioon tekib ainult uriiniga (umbes 80% ravimist eritub muutumatul kujul uriiniga). t 1/2 on 1-1,5 tundi.
Nalidiksiinhapet kasutatakse kuseteede infektsioonide (tsüstiit, püeliit, püelonefriit) korral. Ravim on ette nähtud ka infektsioonide ennetamiseks neerude ja põie operatsioonide ajal.
Ravimi kasutamisel on võimalikud düspeptilised häired, kesknärvisüsteemi erutus, maksafunktsiooni kahjustus ja allergilised reaktsioonid.
Nalidiksiinhape on neerupuudulikkuse korral vastunäidustatud.
Oksoliinhape ja pipemiidhape on sarnased farmakoloogiline toime nalidiksiinhape.
Fluorokinoloonidel on järgmised üldised omadused.
• Selle rühma ravimid inhibeerivad mikroobse raku elutähtsat ensüümi - DNA güraasi (II tüüpi topoisomeraas), mis tagab DNA molekulide ülikerimise ja kovalentse sulgemise. DNA güraasi blokeerimine viib DNA ahelate lahtihaakimiseni ja vastavalt rakusurma (bakteritsiidne toime). Fluorokinoloonide antimikroobse toime selektiivsus tuleneb asjaolust, et II tüüpi topoisomeraas puudub makroorganismi rakkudes.
• Fluorokinoloonidel on lai antibakteriaalse toime spekter. Need on aktiivsed grampositiivsete ja gramnegatiivsete kokkide, Escherichia coli, Salmonella, Shigella, Proteuse, Klebsiella, Helicobacter pylori, Pseudomonas aeruginosa vastu. Üksikud ravimid(tsiprofloksatsiin, ofloksatsiin, lomefloksatsiin) mõjutavad Mycobacterium tuberculosis't. Spiroheedid, listeria ja enamik anaeroobe ei ole fluorokinoloonide suhtes tundlikud.
• Fluorokinoloonid toimivad ekstratsellulaarselt ja intratsellulaarselt lokaliseeritud mikroorganismidele.
• Seda ravimite rühma iseloomustab väljendunud antibiootikumijärgne toime.
• Mikrofloora resistentsus fluorokinoloonide suhtes areneb suhteliselt aeglaselt.
• Fluorokinoloonid tekitavad suukaudsel manustamisel kõrge kontsentratsiooni veres ja kudedes ning biosaadavus ei sõltu toidutarbimisest.
• Fluorokinoloonid tungivad hästi erinevatesse organitesse ja kudedesse: kopsudesse, neerudesse, luudesse, eesnääre jne.
Fluorokinoloone kasutatakse nende suhtes tundlike mikroorganismide poolt põhjustatud kuseteede, hingamisteede, seedetrakti infektsioonide korral. Määrake fluorokinoloonid suu kaudu ja intravenoosselt.
Fluorokinoloonide kasutamisel on võimalikud allergilised reaktsioonid, düspepsia ja unetus. Selle rühma preparaadid pärsivad kõhrekoe arengut, seetõttu on need vastunäidustatud rasedatele ja imetavatele emadele; lastel võib neid kasutada ainult tervislikel põhjustel. Harvadel juhtudel võivad fluorokinoloonid põhjustada kõõlusepõletikku - kõõluste põletikku, mis kehaline aktiivsus võivad põhjustada nende purunemise.
Uutel fluorokinoloonidel (teine põlvkond) on suurem aktiivsus grampositiivsete bakterite, peamiselt pneumokokkide vastu. Levofloksatsiini ja sparfloksatsiini aktiivsus ületab tsiprofloksatsiini ja ofloksatsiini aktiivsust 2–4 korda ning moksifloksatsiini aktiivsust neli või enam korda. On oluline, et uute fluorokinoloonide toime ei erineks penitsilliinitundlike ja penitsilliiniresistentsete pneumokoki tüvede suhtes.
Uuematel fluorokinoloonidel on suurem toime stafülokokkide vastu, mõnel ravimil on mõõdukas toime metitsilliiniresistentsete stafülokokkide vastu.
Kui esimese põlvkonna ravimitel on mõõdukas toime klamüüdia ja mükoplasmade vastu, siis teise põlvkonna ravimid on kõrged, võrreldavad makroliidide ja doksütsükliini aktiivsusega.
Mõnedel uuematel fluorokinoloonidel (moksifloksatsiin jt) on hea toime anaeroobide vastu, sealhulgas Clostridium spp. ja Bacteroides spp., mis võimaldab neid kasutada segainfektsioonide korral monoteraapia režiimis.
Uute fluorokinoloonide peamine kasutusala on kogukonnas omandatud hingamisteede infektsioonid. Samuti on näidatud nende ravimite efektiivsus naha ja pehmete kudede infektsioonide ning urogenitaalinfektsioonide korral.
Uutest fluorokinoloonidest on enim uuritud levofloksatsiini, ofloksatsiini vasakule pööravat isomeeri. Kuna levofloksatsiini on kahes ravimvormis - parenteraalne ja suukaudne, võib seda kasutada raskete infektsioonide korral haiglas. Ravimi biosaadavus on ligi 100%. Levofloksatsiini kliiniline efektiivsus ühekordse manustamisega 250–500 mg / päevas on ravimi oluline eelis, kuid raskes vormis esinevate üldiste nakkusprotsesside korral määratakse levofloksatsiini kaks korda päevas.
Resistentsuse teke levofloksatsiini suhtes on võimalik, kuid resistentsus selle suhtes areneb aeglaselt ja ei ristu teiste antibiootikumidega.
Levofloksatsiin on kõige ohutum fluorokinoloon madal tase hepatotoksilisus. See on koos ofloksatsiini ja moksifloksatsiiniga kesknärvisüsteemile avaldatava toime poolest kõige ohutum. Kõrvaltoimed kohta südame-veresoonkonna süsteem on palju vähem levinud kui teiste fluorokinoloonide puhul. Levofloksatsiini annuse suurendamine 1000 mg-ni päevas ei too kaasa kõrvaltoimete raskuse suurenemist ja nende esinemise tõenäosus ei sõltu patsiendi vanusest.
Üldiselt on levofloksatsiini kasutamisega seotud kõrvaltoimete tase fluorokinoloonide seas madalaim ja selle talutavust peetakse väga heaks.
Nitrofuraani derivaadid
Antimikroobse toimega nitrofuraani derivaate iseloomustab nitrorühma olemasolu furaanisüdamiku positsioonis C5 ja mitmesugused asendajad positsioonis C2.
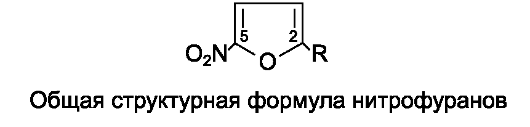
Nitrofuraanide hulka kuuluvad järgmised ravimid.
Nitrofuraal (furatsiliin*), nitrofurantoiin (furadoniin*), furasolidoon, furazidiin (furagin*).
Nitrofuraani derivaatidel on järgmised üldised omadused.
• Võimalus häirida DNA struktuuri. Sõltuvalt kontsentratsioonist on nitrofuraanidel bakteritsiidne või bakteriostaatiline toime.
• Lai spekter antimikroobne toime, mis hõlmab baktereid (grampositiivsed kokid ja gramnegatiivsed pulgad), viirused, algloomad (giardia, trichomonas). Nitrofuraani derivaadid on võimelised toimima teatud antibiootikumide suhtes resistentsete mikroorganismide tüvedele. Nitrofuraanid ei mõjuta anaeroobe ja Pseudomonas aeruginosa. Resistentsus nitrofuraanide suhtes on haruldane.
• Kõrgsagedus kõrvaltoimed, mis ilmnevad ravimite võtmisel.
Nitrofurali kasutatakse peamiselt antiseptikuna (välispidiseks kasutamiseks) mäda-põletikuliste protsesside raviks ja ennetamiseks.
Nitrofurantoiin tekitab uriinis kõrge kontsentratsiooni, mistõttu seda kasutatakse kuseteede infektsioonide korral.
Furasolidoon imendub seedetraktist halvasti ja tekitab kõrge kontsentratsiooni soolestiku luumenis. Furasolidooni kasutatakse bakteriaalse ja algloomade etioloogiaga sooleinfektsioonide korral.
Furatsiini kasutatakse suukaudselt kuseteede infektsioonide korral ning paikselt pesemiseks ja loputamiseks kirurgias.
Nitrofuraani derivaadid võivad põhjustada düspeptilisi häireid, seetõttu tuleb nitrofuraane võtta söögi ajal või pärast seda. Seda ravimite rühma iseloomustavad hepatotoksilised, hematotoksilised ja neurotoksilised toimed. Kell pikaajaline kasutamine nitrofuraani derivaadid võivad põhjustada kopsureaktsioone (kopsuturse, bronhospasm, kopsupõletik).
Nitrofuraani derivaadid on vastunäidustatud raske neeru- ja maksapuudulikkuse, raseduse korral.
8-hüdroksükinoliini derivaadid
To antimikroobsed ained sellesse rühma kuuluvad 5-nitro-8-hüdroksükinoliin - nitroksoliin (5-NOC *). Nitroksoliinil on bakteriostaatiline toime, pärssides selektiivselt bakteriaalse DNA sünteesi. Ravimil on lai antibakteriaalse toime spekter. See imendub seedetraktist hästi ja eritub muutumatul kujul neerude kaudu ning seetõttu akumuleerub ravim suurtes kontsentratsioonides uriiniga.
Nitroksoliini kasutatakse kuseteede infektsioonide raviks ja infektsioonide ennetamiseks pärast neeru- ja kuseteede operatsioone. Tavaliselt taluvad patsiendid ravimit hästi. Mõnikord esineb düspeptilisi nähtusi. Uriin värvitakse ravimiga ravi ajal safranikollase värviga.
Kinoksaliini derivaadid
Teatud kinoksaliini derivaatidel on väljendunud antibakteriaalne toime. Selle rühma ravimite hulka kuuluvad kinoksidiin * ja dioksidiin *. Kinoksaliini derivaatidel on bakteritsiidne toime, mis on seotud võimega aktiveerida peroksüdatsiooniprotsesse, mis põhjustab DNA biosünteesi katkemist ja sügavaid struktuurseid muutusi mikroobiraku tsütoplasmas. Suure toksilisuse tõttu kasutatakse kinoksaliini derivaate ainult tervislikel põhjustel multiresistentsete tüvede põhjustatud raskete anaeroobsete või segatüüpi aeroobsete-anaeroobsete infektsioonide raviks, kui teised antimikroobsed ained on ebaefektiivsed. Määrake kinoksidiin * ja dioksidiin * ainult täiskasvanutele haiglatingimustes. Ravimid on väga mürgised; põhjustada pearinglust, külmavärinaid, kramplikke lihaskontraktsioone jne.
Oksasolidinoonid
Oksasolidinoonid on uus sünteetiliste antibakteriaalsete ainete klass, mis on väga aktiivsed grampositiivsete mikroorganismide vastu.
Linesoliid on esimene selle klassi ravim, mis on registreeritud Vene Föderatsioonis patenteeritud (kaubandusliku) nimetuse Zyvox* all. Seda iseloomustavad järgmised omadused:
• võime pärssida valgusünteesi bakteriraku ribosoomides. Erinevalt teistest antibiootikumidest, mis mõjutavad valgusünteesi, toimib linesoliid varajased staadiumid translatsioon ribosoomide 30S ja 50S alaühikute pöördumatu seondumise teel, mille tulemusena on häiritud 70S kompleksi moodustumine ja peptiidahela moodustumine. See ainulaadne toimemehhanism hoiab ära ristresistentsuse tekke antibiootikumidega, nagu makroliidid, aminoglükosiidid, linkosamiidid, tetratsükliinid, klooramfenikool;
• toime tüüp - bakteriostaatiline. On täheldatud bakteritsiidset toimet Bacteroides fragilis, Clostridium perfringens ja mõned streptokokkide tüved, sealhulgas Streptococcus pneumoniae ja Streptococcus pyogenes;
• toimespekter hõlmab peamisi grampositiivseid patogeene, selliseid probleemseid patogeene nagu metitsilliini- ja glükopeptiidiresistentsed stafülokokid; penitsilliini- ja makroliidresistentsed pneumokokid ja glükopeptiidiresistentsed enterokokid. Linesoliid on gramnegatiivsete bakterite vastu vähem aktiivne;
• suures kontsentratsioonis koguneb bronhopulmonaarsesse epiteeli. Tungib hästi nahka pehmed koed, kopsud, süda, sooled, maks, neerud, kesknärvisüsteem, sünoviaalvedelik, luud, sapipõie. Sellel on 100% biosaadavus;
• vastupanu areneb väga aeglaselt. Pikaajalise parenteraalse kasutamisega (4...6 nädalat) on risk linesoliidi suhtes resistentsuse tekkeks.
Tegevus in vitro ja in vivo, sama hästi kui kliinilised uuringud tõestas linesoliidi efektiivsust haiglas ja kogukonnas omandatud kopsupõletiku korral (kombinatsioonis gramnegatiivsete mikroorganismide vastu aktiivsete antibiootikumidega); vankomütsiiniresistentsete enterokokkide põhjustatud infektsioonid; naha ja pehmete kudede infektsioonidega.
Soovitatav on järgmine annustamisskeem: 600 mg (suukaudselt või intravenoosselt) iga 12 tunni järel.Linesoliidi võib kasutada astmelise raviskeemina esmase parenteraalse manustamisega, seejärel suukaudselt (3.-5. päeval), mis määrab selle farmakoökonoomilise toime.
mõned eelised vankomütsiini alternatiivina. Naha ja pehmete kudede infektsioonide ravis on annus 400 mg iga 12 tunni järel.
On näidatud, et linesolid on hästi talutav nii suukaudsel kui ka intravenoossel manustamisel. Kõige sagedamini teatatud kõrvaltoimed olid seedetraktist (kõhulahtisus, iiveldus, keele värvumine), peavalu ja nahalööve. Tavaliselt ei ole need nähtused tugeva intensiivsusega ja lühiajalised. Linesoliidi kasutamisel rohkem kui kahe nädala jooksul on täheldatud pöörduvat trombotsütopeeniat.
Linesoliid on pöörduv, mitteselektiivne monoamiini oksüdaasi inhibiitor ja võib seetõttu interakteeruda adrenergiliste ainetega, nagu dopamiin, epinefriin ja serotoniinergilised ravimid. Samaaegsel kasutamisel on võimalik suurendada dopamiinergiliste, vasopressorite või sümpatomimeetikumide survet, mis nõuab annuse vähendamist. Linezolid suukaudne suspensioon sisaldab fenüülaliini ja seetõttu tuleb seda fenüülketonuuriaga patsientidel vältida.
37.3. ANTISÜFILIIT
Süüfilis - krooniline suguhaigus mida iseloomustavad naha, limaskestade kahjustused, siseorganid, luud ja närvisüsteem. See on tavaline infektsioon, mis kestab ravimata patsientidel aastaid ja mida iseloomustab laineline kulg, mille ägenemise perioodid vahelduvad varjatud perioodidega.
Süüfilise põhjustajaks on Treponema pallidum (Treponema pallidum). Peamine nakatumise viis on seksuaalne erinevaid vorme ah seks.
Süüfilise ravi toimub spetsiaalsete skeemide järgi.Süüfilise ravimteraapia on reeglina kompleksne, sisaldab antibakteriaalseid ravimeid, samuti aineid, mis mõjutavad organismi immunoloogilist resistentsust.
Süüfilise raviks kasutatakse antibiootikume ja sünteetilisi aineid.
• Antisüüfilised ravimid Antibiootikumid.
• - Bensüülpenitsilliini preparaadid. Bensüülpenitsilliini naatriumi- ja kaaliumisoolad*, prokaiinbensüülpenitsilliin, bensatiinbensüülpenitsilliin (bitsilliin-1*, bitsilliin-5*).
- Tsefalosporiinid.
• Tsefaloridiin (tseporiin*), tseftriaksoon (Longatsef*).
- makroliidid ja asaliidid.
• Erütromütsiin, asitromütsiin (Sumamed *). • Sünteetilised tooted.
- Vismuti preparaadid.
• Biokinool*, bismoverool*.
- Arseeni preparaadid.
• Miarsenool*, atsetarsool (osarsool*).
Peamine koht süüfilise ravis on bensüülpenitsilliini ravimitel. Bensüülpenitsilliini preparaadid on tõhusad süüfilise kõigis etappides. Neile määratakse kursused.
Bensüülpenitsilliini talumatuse korral võib süüfilise raviks kasutada teiste rühmade antibiootikume (vt makroliidid, tsefalosporiinid).
Vismuti ja arseeni preparaate kasutatakse süüfilise erinevate vormide raviks, peamiselt kombinatsioonis penitsilliini rühma antibiootikumidega. Nende ravimite toimemehhanism on tingitud võimest blokeerida ensüümide sulfhüdrüülrühmi mikroorganismide rakkudes ja seeläbi häirida normaalset kulgu. metaboolsed protsessid. Neid manustatakse intramuskulaarselt. Vismutipreparaatide kasutamisel on võimalik gingiviidi ja stomatiidi teke. Arseenipreparaadid põhjustavad kollatõbe, hepatiiti, polüneuriiti.
37.4. TUBERKULOOSIVASTASED RAVIMID
Tuberkuloosivastased ravimid on kemoterapeutilised ained, mis pärsivad Mycobacterium tuberculosis'e kasvu ja aktiivsust.
Tuberkuloos on krooniline retsidiveeruv infektsioon, mille puhul Mycobacterium tuberculosis, nende poolt eritatavad toksiinid ja kudede lagunemissaadused põhjustavad mitmesuguseid häireid normaalses elus ja patoloogilisi muutusi erinevates organites. Sõltuvalt patogeeni lokaliseerimisest eristatakse hingamiselundite tuberkuloosi ja ekstrapulmonaalset tuberkuloosi: nahk, luud ja liigesed, urogenitaalsüsteem, kesknärvisüsteem, kõhuorganid jne.
Tuberkuloosi ravi põhiprintsiibid on järgmised:
• talli saamiseks terapeutiline toime ja võimalike retsidiivide ennetamiseks tuleb tuberkuloosivastaseid ravimeid kasutada pikka aega (6 kuud kuni 1 aasta või rohkem);
• mükobakterite resistentsuse ületamiseks tuleks läbi viia kombineeritud keemiaravi;
• spetsiifiliste tuberkuloosivastaste ravimite ja erinevate farmakoloogiliste rühmade ravimite kompleksne kasutamine (immunostimulaatorid, hormonaalsed ravimid, mukolüütilised ained ja jne).
Kuni 1940. aastateni ei teadnud inimkond tõhusaid tuberkuloosivastaseid ravimeid. 1944. aastal eraldas Waksman streptomütsiini kiirgava seene kultuurivedelikust. Kaks aastat hiljem tehti kindlaks aminosalitsüülhappe (PASA *) tuberkuloosivastane toime ja 1952. aastal tõestati isonikotiinhappe hüdrasiidi derivaatide efektiivsust.
Mycobacterium tuberculosis'e vastu aktiivsel ravimil on märkimisväärne hulk ravimeid, mis erinevad päritolu, keemilise struktuuri, toimemehhanismi ja kliiniline efektiivsus.
Päritolu järgi jagunevad kõik tuberkuloosivastased ravimid antibiootikumideks ja sünteetilisteks antibakteriaalseteks aineteks.
• Tuberkuloosivastased ravimid - antibiootikumid.
- Aminoglükosiidid.
• Streptomütsiinsulfaat*, kanamütsiin, amikatsiin.
- Erinevate keemiliste rühmade antibiootikumid.
• Rifampitsiin, viomütsiin (florimütsiinsulfaat*), tsükloseriin, kapreomütsiin.
• Sünteetilised tuberkuloosivastased ravimid.
- Isonikotiinhappe hüdrasiidi derivaadid.
• Isoniasiid, ftivaziid.
- Para-aminosalitsüülhappe derivaadid.
• PASK * (naatriumparaaminosalitsülaat *), bepask *.
- Isonikotiinhappe tioamiidi derivaadid.
• Etionamiid, protionamiid.
- Erinevate keemiliste rühmade derivaadid.
• Etambutool, pürasiinamiid, tioatsetasoon.
Peamine erinevus sünteetiliste tuberkuloosivastaste ravimite ja antibiootikumide vahel seisneb toimespektris: sünteetilised ravimid on aktiivsed ainult mükobakterite vastu, samas kui antibiootikumidel on lai antimikroobse toime spekter.
Sõltuvalt efektiivsusest ja toksilisusest jagatakse tuberkuloosivastased ravimid kahte rühma.
• Esimese rea preparaadid (baasantibakteriaalne).
Isoniasiid ja selle derivaadid, rifampitsiin, streptomütsiin, PAS*, etambutool.
• Teise valiku ravimid: (reserv).
Tsükloseriin, florimütsiinsulfaat*, kanamütsiin, etionamiid, protionamiid, pürasiinamiid, tioatsetasoon.
Tuberkuloosivastased 1. rea ravimid on aktiivsemad, kuid nende kasutamisel areneb resistentsus Mycobacterium tuberculosis'e vastu üsna kiiresti. Teise rea preparaadid on Mycobacterium tuberculosis'e suhtes vähem aktiivsed; nende peamine omadus on see, et nad toimivad mükobakteritele, mis on muutunud resistentseks esimese rea ravimite suhtes. Lisaks on paljud teise valiku ravimid mürgisemad ja põhjustavad suurema tõenäosusega kõrvaltoimeid.
Kliinilise efektiivsuse järgi jagunevad kõik tuberkuloosivastased ravimid tavaliselt kolme rühma.
• I rühm (kõige tõhusam vahend).
Isoniasiid ja selle derivaadid, rifampitsiin.
• II rühm (keskmise efektiivsusega ravimid).
Streptomütsiin, kanamütsiin, viomütsiin, tsükloseriin, etambutool, etionamiid, protionamiid, pürasiinamiid, ofloksatsiin, lomefloksatsiin.
• III rühm(madala efektiivsusega ravimid).
PAS*, tioatsetasoon.
Isoniasid (isonikotiinhappe hüdrasiid) on isonikotiinhappe derivaatide peamine esindaja, mis on leidnud rakendust tuberkuloosivastaste ravimitena. Isoniasiidi toimemehhanism on inhibeerida mükoolhapete (Mycobacterium tuberculosis'e rakuseina põhikomponent) sünteesiks vajalikke ensüüme.
Kuna mükoolhapete süntees toimub kõige intensiivsemalt kasvavates rakkudes, on isoniasiidil viimastele bakteritsiidne toime; rakkudel puhkeolekus - bakteriostaatiline. Isoniasiidi iseloomustab kemoterapeutilise toime kõrge selektiivsus, kuna makroorganismi kudedes ja ka teistes mikroorganismides puuduvad mükoolhapped.
Isoniasid imendub seedetraktist hästi. Ravimi maksimaalne kontsentratsioon veres registreeritakse 1-4 tundi pärast allaneelamist.
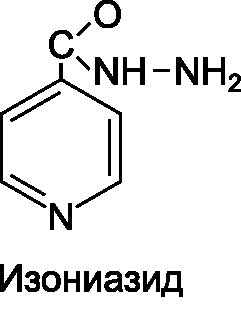
Isoniasiid läbib kergesti BBB-d ja seda leidub erinevates kudedes ja kehavedelikes. Ravim metaboliseerub maksas atsetüülimise teel. Isoniasiidi atsetüülitud vormil ei ole kemoterapeutilist toimet. On kindlaks tehtud, et atsetüülimise kiirus on geneetiliselt määratud. "Kiirete atsetüülijate" puhul on isoniasiidi keskmine poolväärtusaeg alla 1 tunni, "aeglaste atsetüülijate" puhul aga 3 tundi. "Kiirete atsetüülijate" puhul on ravim ette nähtud suuremates annustes. Isoniasiid eritub peamiselt neerude kaudu.
Isoniasiidi kasutatakse kõigi tuberkuloosi vormide korral. Ravimit manustatakse tavaliselt suukaudselt, mõnikord rektaalselt. Vajadusel kasutatakse ravimit intravenoosselt ja intramuskulaarselt.
Isoniasiidi kasutamisel võivad tekkida mitmesugused kõrvaltoimed. Enamasti mõjutavad need kesk- ja perifeerset närvisüsteemi (neuriit, lihastõmblused, unetus, psüühikahäired, mäluhäired). Perifeersete neuropaatiate esinemist seostatakse püridoksaalfosfaadi moodustumise pärssimisega ja kesknärvisüsteemi häiretega - sellest tuleneva GABA puudumisega (eeldatakse, et isoniasiid häirib glutamaadi üleminekut GABA-le).
Isoniasiidil on hepatotoksiline toime, mõnel juhul võib see põhjustada ravimitest põhjustatud hepatiiti. Ravimi kasutamisel on võimalikud allergilised nahareaktsioonid.
Isoniasiidi kõrvaltoimete vältimiseks ja vähendamiseks on soovitatav võtta vitamiine B 1 ja B 6, samuti glutamiinhapet.
Ravim on vastunäidustatud epilepsia, krambihoogude, maksa- ja neerufunktsiooni kahjustuse korral.
Isonikotiinhappe hüdrasiidi derivaatide hulka kuuluvad ka ftivasiid, opiniasiid (lahustuv salusiid *), metasiid.
Rifampitsiin (rifampitsiin *, benemütsiin *) on poolsünteetiline makrotsükliline antibiootikum, millel on lai antibakteriaalse toime spekter. Ravim on aktiivne
Mycobacterium tuberculosis'e ja leepra, mõnede gramnegatiivsete ja grampositiivsete mikroorganismide uurimine. Rifampitsiin inhibeerib bakterite DNA-st sõltuvat RNA polümeraasi, mis põhjustab RNA sünteesi pärssimist bakterites. Rifampitsiin ei mõjuta inimese RNA polümeraasi. Väikestes annustes on ravimil bakteriostaatiline toime, suurtes annustes on see bakteritsiidne.
Rifampitsiin imendub seedetraktist hästi, tühja kõhuga võetuna on biosaadavus 95%, kuid toidu juuresolekul väheneb. Ravim tungib erinevatesse organitesse ja kudedesse, läbib BBB-d. Maksas metaboliseerub rifampitsiin aktiivseks diatsetüülitud metaboliidiks. See eritub organismist uriini ja sapiga.
Rifampitsiini kasutatakse koos isoniasiidi ja teiste tuberkuloosivastaste ravimitega kopsu- ja kopsuväliste tuberkuloosivormide korral. Rifampitsiini manustatakse suu kaudu ja intravenoosselt.
Rifampitsiini kasutamisel on võimalik maksafunktsiooni häire; trombotsütopeenia, aneemia; gripilaadne sündroom (palavik, artralgia, müalgia).
Lisaks põhjustab ravim düspeptilisi häireid, samuti uriini, sülje ja pisaravedeliku värvimist oranžiks.
Streptomütsiin ja kanamütsiin on aminoglükosiidide rühma kuuluvad antibiootikumid (vt ptk 37). Neid ravimeid kasutatakse peamiselt äsja registreeritud kopsutuberkuloosi ja teiste elundite tuberkuloossete kahjustuste raviks. Mycobacterium tuberculosis'e resistentsus aminoglükosiidide suhtes areneb üsna kiiresti.
Streptomütsiinsulfaati * manustatakse intramuskulaarselt, intratrahheaalselt ja intrakavernoosselt ning kanamütsiinsulfaati * - intramuskulaarselt. Need ravimid on väga mürgised.
Viomütsiin (florimütsiinsulfaat *) - antibiootikum, kiirgavate seente jääkprodukt Streptomyces floridae. Ravimil on bakteriostaatiline toime mycobacterium tuberculosis'ele, see on aktiivne ka mõnede grampositiivsete ja gramnegatiivsete bakterite vastu. "Reserv" ravim tuberkuloosi erinevate vormide ja lokalisatsioonide ravis. Viomütsiini manustatakse intramuskulaarselt. Ravimi kasutamisel võib tekkida ototoksiline toime, mistõttu seda ei saa kombineerida aminoglükosiidide rühma antibiootikumidega.
Tsükloseriin on antibiootikum, mis moodustub elutähtsa tegevuse käigus. Streptomyces orchidaceus. Praegu toodetakse tsükloseriini sünteetiliselt.
Keemilise struktuuri järgi on see D-4-amino-3-isoksasolidinoon. Tsükloseriin toimib bakteritsiidselt, häirides mikroorganismide rakuseina sünteesi (vt ptk 37). Ravimil on lai antibakteriaalse toime spekter: see pärsib grampositiivseid ja gramnegatiivseid baktereid. Selle kõige väärtuslikum omadus on aktiivsus Mycobacterium tuberculosis'e vastu. Resistentsus tsükloseriini suhtes areneb aeglaselt.
Suukaudsel manustamisel imendub tsükloseriin hästi, tekitades kõrge plasmakontsentratsiooni. Tungib erinevatesse kudedesse ja kehavedelikesse, läbib BBB-d. Eritub neerude kaudu. Ravimit kasutatakse sees.
Tsükloseriini kasutamisel tekivad sageli kõrvaltoimed. Neist levinumad on neurotoksilised reaktsioonid (peavalu, pearinglus, desorientatsioon; raskematel juhtudel nägemiskahjustus, depressioon, psühhoos). Nende häirete vältimiseks on ette nähtud püridoksiin ja glutamiinhape.
Et ja m but t about l on sünteetiline tuberkuloosivastane aine. Keemilise struktuuri järgi on see etüleendiimiini derivaat.
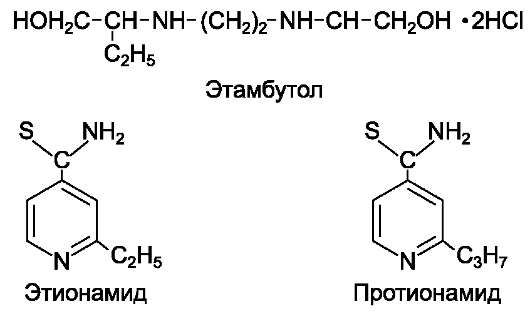
Etambutoolil on väljendunud tuberkulostaatiline toime, see ei mõjuta teisi mikroorganisme. Ravim pärsib streptomütsiini ja isoniasiidi suhtes resistentsete mükobakterite kasvu.
Ravim imendub seedetraktist hästi, tungib enamikesse kudedesse ja kehavedelikesse, läbib BBB-d. Eritub peamiselt neerude kaudu. Määrake see sees.
Etambutooli kasutamisel võib köha suureneda, röga hulk suureneda, düspeptilised sümptomid, peavalu ja nägemisteravus halveneda. Ravi käigus on vaja süstemaatiliselt jälgida nägemisteravust, värvitaju ja muid silma seisundi näitajaid.
Etionamiid ja protionamiid (treventix*) on sarnase struktuuriga sünteetilised preparaadid, isonikotiinhappe derivaadid.
Ravimitel on bakteriostaatiline toime. Need pärsivad resistentsuse teket teiste tuberkuloosivastaste ravimite suhtes ja omavad nende suhtes sünergiat.
Etionamiid ja protionamiid imenduvad seedetraktist hästi, tungivad paljudesse organitesse ja kudedesse ning võivad tungida ka kapseldatud moodustistesse ja õõnsustesse. Metaboliseerub maksas, eritub neerude kaudu.
Ravimite kasutamisega võivad kaasneda seedetrakti häired, maksafunktsiooni häired, unisus, hallutsinatsioonid.
P ja raz ja n ja m ja d - sünteetiline aine, millel on tuberkulostaatiline toime. Ravim ei mõjuta teisi mikroorganisme. Resistentsus pürasiinamiidi suhtes areneb kiiresti.
Ravim imendub seedetraktist hästi, tungib kiiresti kõikidesse kudedesse ja bioloogilistesse vedelikesse, metaboliseerub peamiselt maksas ja eritub neerude kaudu.
Ravimi kasutamisel tekivad sageli düspeptilised sümptomid. Pürasiinamiid võib põhjustada hüperurikeemiat, mis väljendub artralgia ja müalgiana. Lisaks on ravimil hepatotoksiline toime.
Ofloksatsiin ja lomefloksatsiin on sünteetilised antibakteriaalsed ained fluorokinoloonide rühmast, mis on aktiivsed Mycobacterium tuberculosis'e vastu (vt ptk 37). Ravimeid kasutatakse kompleksne teraapia tuberkuloos.
Aminosalitsüülhapet (PASA*) kasutatakse naatriumi- või kaltsiumisoolana.
Ravimil on tuberkulostaatiline toime. PAS* tuberkulostaatiline toime põhineb antagonismil para-aminobensoehappega, mis on mükobakterite kasvufaktor. PAS* toimib ainult mükobakteritele, mis on aktiivses paljunemisseisundis.
Suukaudsel manustamisel imendub ravim hästi, kuid sellel on väljendunud ärritav toime seedetrakti limaskestale. Metaboliseerub maksas ja osaliselt seedetraktis. Eritub uriiniga.
PASK-i kasutatakse kombineeritud keemiaravi osana kõigi tuberkuloosi vormide puhul.
PAS-i kõige sagedasemad kõrvaltoimed väljenduvad düspeptiliste häiretena (iiveldus, oksendamine, kõhulahtisus). Lisaks on võimalikud allergilised tüsistused.
Tioatsetasoon (tibon*) on sünteetiline aine, millel on bakteriostaatiline toime Mycobacterium tuberculosis'e ja pidalitõve tekitaja vastu. Kõrge toksilisuse tõttu kasutatakse ravimit piiratud määral: tavaliselt määratakse seda koos isoniasiidi, streptomütsiini ja teiste tuberkuloosivastaste ravimitega, et suurendada. terapeutiline toime ja Mycobacterium tuberculosis'e resistentsete vormide tekkimise võimaluse vähendamine. Ravimit võetakse suu kaudu.
Tioatsetasooni ravis on võimalik peavalu, iiveldus, dermatiit, isutus. Harvadel juhtudel võivad esineda hematoloogilised häired.